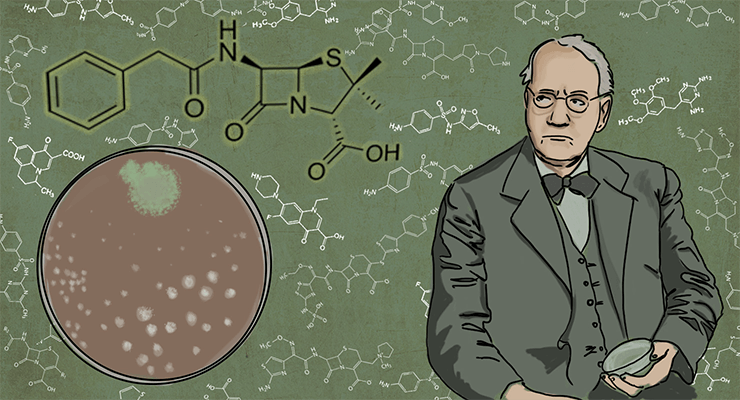
4997. Лечение антибиотиками болезней человека, вызванных болезнетворными микроорганизмами, со временем становится малоэффективным. Необходимо вести поиски новых лекарственных препаратов. Объясните почему.
1) Мутации приводят к возникновению особей с измененными свойствами
2) Устойчивость к антибиотикам — полезный признак микроорганизмов, который поддерживается естественным отбором (особи с таким признаком выживают и размножаются)
3) Микроорганизмы обладают высокой скоростью размножения, вследствие чего возникшие полезные мутации быстро распространяются и закрепляются: за короткое время формируется новая популяция, которая устойчива к действию антибиотика (обладает невосприимчивостью к нему)
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке 
При обращении указывайте id этого вопроса — 4997.
26
1. Какие
формы естественного отбора изменяют норму реакции признака? Ответ поясните.
1)
Движущий отбор – норма реакции признака
сменяется постепенно, появляются особи с крайним значением признака (либо в
сторону уменьшения, либо в сторону увеличения);
2)
Дизруптивный (разрывающий) – норма реакции
разрывается, остаются особи с крайними значениями признака, а особи со средним
значением признака вытесняются;
3)
Дестабилизирущий отбор – норма реакции
признака расширяется; преимущество получают особи с более широкой нормой
реакции.
2. Что
такое борьба за существование по Ч. Дарвину? Каковы причины возникновения
борьбы за существование?
1)
борьба за существование – это совокупность
сложных взаимоотношений между организмами и внешней средой, в результате
которой погибают одни особи и выживают другие;
2)
способность организмов к неограниченному
размножению (размножение организмов в геометрической прогрессии);
3)
ограниченность природных ресурсов,
ограниченность средств к жизни.
3. Охарактеризуйте
социально-экономические предпосылки эволюционного учения Ч. Дарвина.
1)
Интенсивное развитие капитализма в первой
половине XIX века в Англии привело к
быстрому росту городов, городского населения; быстрый рост городов требовал
быстрого повышения продуктивности сельского хозяйства;
2)
Спрос промышленности на сырьё и населения
на продукты питания способствовал развитию селекции; проводились научные
экспедиции;
3)
Появились экономическое учение А. Смита о
свободной конкуренции и Т. Мальтуса о народонаселении.
4. Какие
виды изменчивости описал Ч. Дарвин в своей теории как один из движущих факторов
эволюции? Ответ поясните.
1)
Определённая (групповая) – появление
сходных признаков у особей одного вида под влиянием одинаковых условий среды;
ненаследственная изменчивость;
2)
Неопределённая (индивидуальная) –
возникновение различных изменений у особей одного вида под влиянием сходных условий;
наследственная изменчивость;
3)
Соотносительная ( корреляционная) –
изменение одного органа влечёт за собой изменение других органов;
наследственная изменчивость.
5. Ч.
Дарвин создал эволюционную теорию. К чему сводится учение Дарвина? Укажите не
менее четырёх положений.
1)
Каждая особь того или иного вида обладает
индивидуальностью ( изменчивость);
2)
Черты индивидуальности (хотя и не все)
могут передаваться по наследству (наследственность);
3)
Особи производят большее количество
потомков, чем доживает до половой зрелости и начала размножения, то есть в
природе идёт борьба за существование;
4)
Преимущество в борьбе за существование
остаётся за наиболее приспособленными особями, которые имеют больше шансов
оставить после себя потомство (естественный отбор);
5)
В результате естественного отбора
происходит постепенное усложнение уровней организации жизни и возникновение
видов.
6. Лечение
антибиотиками болезней человека, вызванных микроорганизмами со временем
становится малоэффективным. Необходимо вести поиски новых лекарственных
препаратов. Объясните с точки зрения эволюционного процесса, как развивается
устойчивость к антибиотикам.
1)
В результате мутаций возникают
микроорганизмы с устойчивостью к антибиотикам, что оказывается полезным
признаком;
2)
Микроорганизмы обладают высокой скоростью
размножения, возникшие полезные мутации быстро распространяются;
3)
В результате борьбы за существование и
естественного отбора возникает новая популяция, невосприимчивая к антибиотику.
7. Почему
ныне живущую кистепёрую рыбу латимерию нельзя считать предком земноводных?
Приведите не менее трёх доказательств.
1)
Предки земноводных жили в пресных
водоёмах, в прибрежной зоне, а латимерия приспособлена к жизни в глубинах
солёных водоёмов (океана);
2)
Предки земноводных могли дышать
атмосферным кислородом с помощью лёгких, а латимерия атмосферным кислородом не
дышит;
3)
Предки земноводных могли передвигаться по
дну водоёма с помощью парных плавников, латимерия с помощью парных плавников
может только плавать в воде.
поделиться знаниями или
запомнить страничку
- Все категории
-
экономические
43,622 -
гуманитарные
33,648 -
юридические
17,917 -
школьный раздел
611,562 -
разное
16,897
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Согласно историческим источникам, еще много тысячелетий назад наши предки, столкнувшись с болезнями, вызываемыми микроорганизмами, боролись с ними доступными средствами. Со временем человечество начало понимать, почему те или иные используемые издревле лекарства способны воздействовать на определенные болезни, и научилось изобретать новые лекарства. Сейчас объем средств, используемых для борьбы с патогенными микроорганизмами, достиг особо крупных масштабов, по сравнению даже с недавним прошлым. Давайте рассмотрим, как на протяжении своей истории человек, порой того не подозревая, использовал антибиотики, и как, по мере накопления знаний, использует их сейчас.
Бактерии появились на нашей планете, по разным оценкам, приблизительно 3,5–4 миллиарда лет назад, задолго до эукариот [1]. Бактерии, как и все живые существа, взаимодействовали друг с другом, конкурировали и враждовали. Мы не можем точно сказать, использовали ли они уже тогда антибиотики, чтобы победить других прокариот в схватке за лучшую среду или питательные вещества. Но существуют доказательства наличия генов, кодирующих устойчивость к бета-лактаму, тетрациклину и гликопептидным антибиотикам, в ДНК бактерий, которые находились в древнем пермафросте возрастом 30 000 лет [2].
С момента, который принято считать официальным открытием антибиотиков, прошло чуть менее ста лет, но проблема создания новых антимикробных препаратов и использования уже известных при условии быстро возникающей резистентности к ним тревожит человечество не последние пятьдесят лет. Неспроста в своей Нобелевской речи первооткрыватель пенициллина Александр Флеминг предупреждал, что к использованию антибиотиков нужно подходить серьезно.
Так же, как и момент открытия антибиотиков человечеством на несколько миллиардов лет отсрочен от изначального их появления у бактерий, так и история использования человеком антибиотиков началась задолго до их официального открытия. И речь идет не о предшественниках Александра Флеминга, живших в 19 веке, а о совсем далеких временах.
Использование антибиотиков в древности
Еще в Древнем Египте плесневелый хлеб использовали для дезинфекции порезов (видео 1). Хлеб с плесневыми грибками в лечебных целях применяли и в других странах и, видимо, вообще во многих древних цивилизациях. Например, в Древней Сербии, Китае и Индии для предотвращения развития инфекций его прикладывали к ранам. Судя по всему, жители этих стран независимо друг от друга пришли к выводу о целебных свойствах плесени и использовали ее для лечения ран и воспалительных процессов на коже. Древние египтяне прикладывали к гнойникам на коже головы корки плесневелого пшеничного хлеба и считали, что использование этих средств поможет умилостивить духов или богов, ответственных за болезни и страдания.
Видео 1. Причины появления плесени, ее вред и польза, а также применение в медицине и перспективы использования в будущем
Жители Древнего Египта для лечения ран использовали не только хлеб с плесенью, но и самостоятельно изготовленные мази. Есть информация о том, что примерно в 1550 г. до н.э. они готовили смесь из свиного сала и меда, которую наносили на раны и перевязывали специальной тканью. Такие мази обладали некоторым антибактериальным эффектом в том числе благодаря содержащейся в меде перекиси водорода [3], [4]. Египтяне не были первопроходцами в использовании меда — первым упоминанием о его целебных свойствах считают запись на шумерской табличке, датируемую 2100–2000 гг. до н.э., где говорится, что мед можно использовать как лекарство и мазь. И Аристотель также отмечал, что мед хорош для лечения ран [3].
В процессе исследования костей мумий древних нубийцев, живших на территории современного Судана, ученые обнаружили в них большую концентрацию тетрациклина [5]. Возраст мумий составлял примерно 2500 лет, и, скорее всего, высокие концентрации антибиотика в костях не могли появиться случайно. Даже в останках четырехлетнего ребенка его количество была очень высоко. Ученые предполагают, что эти нубийцы на протяжении длительного времени потребляли тетрациклин. Скорее всего, его источником были бактерии Streptomyces или другие актиномицеты, содержащиеся в зернах растений, из которых древние нубийцы делали пиво.
В борьбе с инфекциями люди по всему миру использовали и растения. Сложно понять, когда именно некоторые из них начинали применять, из-за отсутствия письменных или других материальных свидетельств. Некоторые растения использовали потому, что человек методом проб и ошибок узнавал об их противовоспалительных свойствах. Другие растения использовали в кулинарии, и вместе со вкусовыми свойствами они обладали и антимикробным действием.
Так обстоит дело с луком и чесноком. Эти растения с давних пор использовали в приготовлении пищи и медицине. Об антимикробных свойствах чеснока знали еще в Китае и Индии [6]. А не так давно ученые выяснили, что народная медицина не зря использовала чеснок — его экстракты угнетают Bacillus subtilis, Escherichia coli и Klebsiella pneumonia [7].
В Корее издревле для лечения желудочно-кишечных инфекций, вызываемых сальмонеллой, используют лимонник китайский Schisandra chinensis. Уже в наши дни, после проверки действия его экстракта на эту бактерию, оказалось, что лимонник действительно обладает антибактериальным действием [8]. Или, к примеру, на присутствие антибактериальных веществ проверили специи, которые широко используются по всему миру. Получилось, что душица, гвоздика, розмарин, сельдерей и шалфей угнетают такие патогенные микроорганизмы, как Staphylococcus aureus, Pseudomonas fluorescens и Listeria innocua [9]. На территории Евразии народы часто заготавливали ягоды и, естественно, использовали их в том числе и в лечении. Научные исследования подтвердили, что некоторые ягоды обладают антимикробной активностью. Фенолы, особенно эллаготанины, содержащиеся в плодах морошки и малины, ингибируют рост кишечных патогенных микроорганизмов [10].
XX век
1940–1960-е годы XX века называют «золотой эрой» открытия антибиотиков. В то время, чтобы получить новое вещество, обладающее антибиотической активностью, можно было взять пробу почвы, выделить из нее микроорганизмы и изучать их. На этом же объекте исследования можно было испытывать новосинтезированные или выделенные из других микроорганизмов антибиотики. В 1980-х начала свое развитие комбинаторная химия, а в 1990-х ее методы стали использовать фармкомпании, в том числе и для поиска новых антибиотиков.
Официально, «золотая эра антибиотиков» начинается с открытия пенициллина. Это произошло в 1928 году, и первооткрывателем официально считают британского бактериолога Александра Флеминга (рис. 1). Кстати, ту самую чашку Петри, благодаря которой он сделал открытие и в дальнейшем получил Нобелевскую премию, вместе с той самой плесенью не так давно продали на аукционе за 14 тысяч долларов.
Строго говоря, Александр Флеминг (о котором рассказывает статья «Победитель бактерий» [12]) является первооткрывателем пенициллина лишь официально. У него были предшественники, о которых также можно прочитать на «биомолекуле»: «Эволюция наперегонки, или почему антибиотики перестают работать» [13].
Рисунок 1. Александр Флеминг.
Поначалу открытие Флеминга не использовалось для лечения пациентов и продолжало свою жизнь исключительно за дверями лаборатории. К тому же, как сообщали современники Флеминга, он не был хорошим оратором и не мог убедить общественность в полезности и важности пенициллина. Вторым рождением этого антибиотика можно назвать его переоткрытие учеными из Великобритании Эрнстом Чейном и Говардом Флори в 1940–1941 гг.
В СССР тоже использовали пенициллин, причем если в Великобритании применяли не особенно производительный штамм, то советский микробиолог Зинаида Ермольева в 1942 году обнаружила таковой и даже сумела наладить производство антибиотика в условиях войны [14]. Наиболее активным штаммом был Penicillium crustosum, и поэтому поначалу выделенный антибиотик называли пенициллин-крустозин. Его использовали на одном из фронтов во время Великой Отечественной войны для профилактики послеоперационных осложнений и лечения ран [15].
Зинаида Ермольева написала небольшую брошюру, в которой рассказала о том, как в СССР был открыт пенициллин-крустозин и как происходил поиск других антибиотиков: «Биологически активные вещества» [15].
В Европе пенициллин тоже использовали для лечения военных, причем после того, как этот антибиотик начали применять в медицине, он оставался привилегией исключительно военных [16]. Но после пожара 28 ноября 1942 года в ночном клубе Бостона пенициллин стали применять и для лечения гражданских пациентов. У всех пострадавших были ожоги разной степени сложности, и в то время такие пациенты зачастую умирали от бактериальных инфекций, вызываемых, например, стафилококками. Компания Merck & Co. отправила пенициллин в госпитали, где содержались пострадавшие при этом пожаре, и успех лечения поставил пенициллин в центр внимания общественности. К 1946 году он стал широко использоваться в клинической практике.
Доступным для общественности пенициллин оставался вплоть до середины 50-х годов XX века. Естественно, находясь в неконтролируемом доступе, этот антибиотик зачастую использовался неуместно. Есть даже примеры пациентов, которые считали, что пенициллин — чудо-средство от всех человеческих болезней, и применяли его даже для «лечения» того, что ему по природе своей не способно поддаться. Но в 1946 году в одном из американских госпиталей заметили, что 14% взятых от больных пациентов штаммов стафилококка были устойчивы к пенициллину. А в конце 1940-х этот же госпиталь сообщил, что процент резистентных штаммов вырос до 59%. Интересно заметить, что первые сведения о том, что к пенициллину возникает устойчивость, появились в 1940 году — еще до того, как антибиотик стали активно использовать [17].
До открытия в 1928 году пенициллина, были, конечно, и открытия других антибиотиков. На рубеже XIX–XX веков заметили, что голубой пигмент бактерии Bacillus pyocyaneus способен убивать множество патогенных бактерий, таких как холерный вибрион, стафилококки, стрептококки, пневмококки. Он был назван пиоционазой, но открытие не послужило основой для разработки препарата, потому что вещество было токсично и нестабильно.
Первым коммерчески доступным антибиотиком стал препарат «Пронтосил», который разработал немецкий бактериолог Герхард Домагк в 1930-х годах [18]. Есть документальные свидетельства, что первым вылеченным человеком оказалась его собственная дочь, которая долго страдала от заболевания, вызванного стрептококками. В результате лечения она выздоровела всего за несколько дней. Сульфаниламидные препараты, к которым относится и «Пронтосил», широко использовали во время Второй мировой войны страны антигитлеровской коалиции для предотвращения развития инфекций.
Вскоре после открытия пенициллина, в 1943 году, Альберт Шац, молодой сотрудник в лаборатории Зельмана Ваксмана [19], выделил из почвенной бактерии Streptomyces griseus вещество, обладающее противомикробной активностью. Этот антибиотик, названный стрептомицином, оказался активным против многих распространенных в то время инфекций, в том числе туберкулеза и чумы.
И все же, примерно до 1970-х годов никто серьезно не задумывался о развитии резистентности к антибиотикам. Затем были замечены два случая заболевания гонореей и бактериальным менингитом, когда бактерия, устойчивая к лечению пенициллином или антибиотиками пенициллинового ряда, вызывала смерть пациента. Эти события ознаменовали момент, когда с десятилетиями удачного лечения заболеваний было покончено.
Надо понимать, что бактерии — это живые системы, поэтому они изменчивы и со временем способны выработать резистентность к любому антибактериальному препарату (рис. 2). Например, к линезолиду бактерии не могли выработать устойчивость на протяжении 50 лет, но все-таки сумели приспособиться и жить в его присутствии [20]. Вероятность развития антибиотикорезистентности в одном поколении бактерий составляет 1:100 млн. К действию антибиотиков они приспосабливаются по-разному. Это может быть усиление клеточной стенки, которую, к примеру, использует Burkholderia multivorans, вызывающая пневмонию у людей с иммунодефицитами [21]. Некоторые бактерии, такие как Campylobacter jejuni, которая вызывает энтероколит, очень эффективно «выкачивают» антибиотики из клеток при помощи специализированных белковых насосов [22], и поэтому антибиотик не успевает подействовать.
Подробнее о способах и механизмах приспособления микроорганизмов к антибиотикам мы уже писали: «Эволюция наперегонки, или почему антибиотики перестают работать» [13]. А на сайте проекта онлайн-образования Coursera есть полезный курс про антибиотикорезистентность Antimicrobial resistance — theory and methods. В нем достаточно подробно рассказывается об антибиотиках, механизмах устойчивости к ним и путях распространения резистентности.
Рисунок 2. Один из путей возникновения антибиотикорезистентности.
Чтобы увидеть рисунок в полном размере, нажмите на него.
Первый случай возникновения метициллинустойчивого золотистого стафилококка (MRSA) зафиксировали в Великобритании в 1961 году, а в США — немного позднее, в 1968-м [23]. Про золотистого стафилококка мы чуть подробнее поговорим дальше, но в контексте скорости выработки у него резистентности стоит отметить, что в 1958 году против этой бактерии стали использовать антибиотик ванкомицин. Он был способен работать с тем штаммами, которые не поддавались воздействию метициллина. И до конца 1980-х годов считалось, что к нему резистентность должна вырабатываться дольше или вообще не вырабатываться. Однако в 1979 и 1983 годах, по прошествии всего пары десятков лет, в разных частях мира были зафиксированы случаи устойчивости и к ванкомицину [24].
Похожий тренд соблюдался и для других бактерий, а некоторые оказались способными выработать резистентность вообще за год. Но кто-то приспосабливался немного медленнее, например, в 1980-х годах только 3–5% S. pneumonia были устойчивы к пенициллину, а в 1998 году — уже 34%.
XXI век — «кризис инноваций»
За последние 20 лет многие большие фармкомпании — например, Pfizer, Eli Lilly and Company и Bristol-Myers Squibb — сократили число разработок или вообще закрыли проекты по созданию новых антибиотиков. Это можно объяснить не только тем, что стало сложнее искать новые вещества (потому что все, которые было легко найти, уже нашли), но и потому что есть другие востребованные и более прибыльные области, например, создание лекарств для лечения онкологических заболеваний или депрессии.
Тем не менее, время от времени то один, то другой коллектив ученых или компания сообщает, что они открыли новый антибиотик, и заявляет, что «вот он уж точно победит все бактерии/некоторые бактерии/определенный штамм и спасет мир». После этого зачастую ничего не происходит, и такие высказывания вызывают у общественности только скепсис. Ведь помимо тестирования антибиотика на бактериях в чашке Петри, нужно провести испытания предполагаемого вещества на животных, а затем и на людях. Это занимает много времени, таит в себе немало подводных камней, и обычно на одной из этих фаз открытие «чудесного антибиотика» сменяется закрытием.
Для того чтобы найти новые антибиотики, применяют различные методы: как классической микробиологии, так и более новые — сравнительной геномики, молекулярной генетики, комбинаторной химии, структурной биологии. Некоторые предлагают отойти от этих «привычных» методов и обратиться к знаниям, накопленным на протяжении истории человечества. Например, в одной из книг Британской библиотеки ученые заметили рецепт бальзама от глазных инфекций, и им стало интересно, на что он способен сейчас. Рецепт датировался X веком, поэтому вопрос — будет работать или нет? — был действительно интригующим. Ученые взяли именно те ингредиенты, которые были указаны, смешали в нужных пропорциях и проверили на метициллинрезистентном золотистом стафилококке (MRSA). К удивлению исследователей, более 90% бактерий были убиты этим бальзамом. Но важно заметить, что такой эффект наблюдался только при совместном использовании всех ингредиентов [25], [26].
Действительно, порой антибиотики природного происхождения работают не хуже современных, но их состав настолько сложен и зависит от многих факторов, что быть точно уверенным в каком-то определенном результате затруднительно. Также, невозможно сказать, замедляется ли скорость выработки устойчивости к ним или нет. Поэтому их не рекомендуют использовать как замену основной терапии, а как дополнение под строгим контролем врачей [20].
Проблемы резистентности — примеры болезней
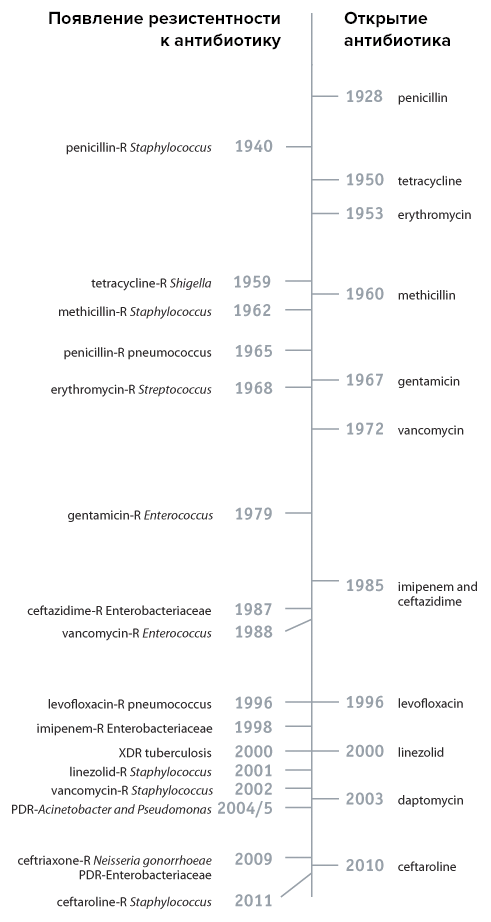
Невозможно дать полную картину резистентности микроорганизмов к антибиотикам, потому как эта тема многогранна и, несмотря на несколько поутихший интерес со стороны фармкомпаний, достаточно активно исследуется. Соответственно, очень быстро появляется информация о все новых и новых случаях устойчивости к антибиотикам. Поэтому мы ограничимся лишь несколькими примерами для того, чтобы хотя бы поверхностно показать картину происходящего (рис. 3).
Рисунок 3. Временная шкала открытия некоторых антибиотиков и выработки устойчивости к ним.
Туберкулез: риск в современном мире
Туберкулез особенно распространен в Центральной Азии, Восточной Европе и России, и то, что у туберкулезных микробов (Mycobacterium tuberculosis) возникает устойчивость не только к определенным антибиотикам, но и к их комбинациям, должно вызывать тревогу.
У пациентов с ВИЧ из-за пониженного иммунитета нередко возникают оппортунистические инфекции, вызываемые микроорганизмами, которые в норме могут без вреда присутствовать в организме человека. Одной из них является туберкулез, который к тому же отмечен как основная причина смерти ВИЧ-положительных пациентов по всему миру. О распространенности туберкулеза по регионам мира можно судить из статистики — у пациентов с ВИЧ, заболевших туберкулезом, если они проживают в Восточной Европе, риск умереть в 4 раза выше, чем если бы они жили в Западной Европе или даже Латинской Америке. Конечно, стоит отметить, что на эту цифру влияет то, насколько в медицинской практике региона принято проводить тесты на восприимчивость пациентов к лекарствам. Это позволяет применять антибиотики только при необходимости.
За ситуацией с туберкулезом наблюдает и ВОЗ. В 2017 году она выпустила доклад о выживаемости при туберкулезе и его мониторинге в Европе. Существует стратегия ВОЗ по ликвидации туберкулеза, и поэтому пристальное внимание обращается на регионы с высоким риском заражения этим заболеванием.
Туберкулез унес жизни таких мыслителей прошлого, как немецкий писатель Франц Кафка и норвежский математик Н.Х. Абель. Однако это заболевание вызывает тревогу и сегодня, и при попытке взглянуть в будущее. Поэтому и на общественном, и на государственном уровнях стоит прислушиваться к стратегии ВОЗ и стараться снизить риски заражения туберкулезом.
В докладе ВОЗ подчеркнуто, что с 2000 года фиксируется меньше случаев заражения туберкулезом: в период с 2006 по 2015 годы число случаев уменьшалось на 5,4% в год, а в 2015 уменьшилось на 3,3%. Тем не менее, несмотря на такой тренд, ВОЗ призывает с вниманием относиться к проблеме антибиотикорезистентности Mycobacterium tuberculosis, и, используя методы гигиены и постоянный мониторинг населения, уменьшать число случаев инфицирования.
Устойчивая гонорея
Американское агентство Центры по контролю и профилактике заболеваний (CDC) подсчитали, что в США ежегодно фиксируется более 800 тысяч случаев заболевания гонореей, а во все мире, по оценке ВОЗ, — 78 миллионов случаев. Это инфекционное заболевание вызывается гонококком Neisseria gonorrhoeae. В проведенных исследованиях за период с 2009 по 2014 годы показано, что многие штаммы гонококка резистентны к препарату первой линии — ципрофлоксацину, а также увеличивается число устойчивых штаммов к азитромицину и препаратам группы цефалоспоринов широкого спектра действия. В большинстве стран никакие другие антибиотики, кроме цефалоспоринов, не способны воздействовать на гонококка, но уже и к ним возрастает устойчивость. Недавно выявили три случая, когда гонококк оказывался устойчивым ко всем известным препаратам, применяемым для лечения гонореи [27].
Масштабы резистентности других бактерий
Примерно 50 лет назад начали появляться штаммы золотистого стафилококка, устойчивые к антибиотику метициллину (MRSA). Инфекции, вызванные метициллинрезистентным золотистым стафилококком, ассоциированы с бóльшим количеством смертей, чем инфекции, вызванные метициллинчувствительным стафилококком (MSSA). Большинство из MRSA также устойчиво и к другим антибиотикам. В настоящее время они распространены и в Европе, и в Азии, и в обеих Америках, и в Тихоокеанском регионе [28]. Эти бактерии чаще других становятся устойчивыми к антибиотикам и в США убивают 12 тысяч людей за год [29]. Есть даже факт, что в США MRSA в год уносит больше жизней, чем ВИЧ/СПИД, болезнь Паркинсона, эмфизема легких и убийства вместе взятые [30], [31].
В период с 2005 по 2011 год стали фиксировать меньше случаев заражения MRSA как госпитальной инфекцией. Это связано с тем, что в медицинских учреждениях взяли под строгий контроль соблюдение гигиенических и санитарных норм. Но в общей популяции такой тренд, к сожалению, не сохраняется.
Энтерококки, устойчивые к действию антибиотика ванкомицина — большая беда. Они не так широко распространены на планете, по сравнению с MRSA, но в США каждый год фиксируется около 66 тысяч случаев заражения Enterococcus faecium и, реже, E. faecalis. Они являются причиной большого спектра заболеваний и особенно среди пациентов медицинских учреждений, то есть они — причина госпитальных инфекций. При заражении энтерококком около трети случаев приходится на штаммы, устойчивые к ванкомицину.
Пневмококк Streptococcus pneumoniae является причиной бактериальной пневмонии и менингита. Чаще заболевания развиваются у людей старше 65 лет. Возникновение резистентности усложняет лечение и в итоге приводит к 1,2 миллионам случаев заболевания и 7 тысячам смертей ежегодно. Пневмококк резистентен к амоксициллину и азитромицину. К менее распространенным антибиотикам он тоже выработал устойчивость, и в 30% случаев резистентен к одному или нескольким применяемым в лечении препаратам. Надо заметить, что даже если присутствует небольшой уровень устойчивости к антибиотику, это не снижает эффективность от лечения им. Использование препарата становится бесполезным в случае, если количество резистентных бактерий превышает определенный порог. Для внебольничных пневмококковых инфекций этот порог составляет 20–30% [32]. В последнее время стало происходить меньше случаев заражения пневмококком, потому что в 2010 году создали новую версию вакцины PCV13, которая действует против 13 штаммов S. pneumoniae.
Пристальное внимание должно оказываться не только бактериям, которые уже развивают или развили резистентность, но и тем, которые пока не приобрели устойчивость. Потому что со временем и они могут измениться и начать вызывать более сложные формы заболеваний.
Внимание к нерезистентным бактериям можно объяснить и тем, что, даже легко поддаваясь лечению, эти бактерии играют роль в развитии инфекций у пациентов с ослабленным иммунитетом — ВИЧ-положительных, проходящих химиотерапию, недоношенных и переношенных новорожденных, у людей после операции и трансплантации [33]. И так как этих случаев происходит достаточное количество —
- во всем мире в 2014 году было проведено около 120 тысяч трансплантаций;
- только в США ежегодно проходят химиотерапию 650 тысяч человек, однако не у всех есть возможность использовать препараты для борьбы с инфекциями;
- в США 1,1 миллиона человек — ВИЧ-положительные, в России — чуть меньше, официально 1 млн;
— то есть шанс, что со временем устойчивость появится и у тех штаммов, которые пока не вызывают опасений.
Госпитальные, или внутрибольничные, инфекции все чаще встречаются в наше время. Это те инфекции, которыми люди заражаются в больницах и других медицинских учреждениях при госпитализации и просто при посещении.
В США в 2011 году было зафиксировано более 700 тысяч заболеваний, вызываемых бактериями рода Klebsiella [34]. Это, в основном, внутрибольничные инфекции, которые приводят к довольно обширному спектру заболеваний, таких как пневмония, сепсис, раневые инфекции. Как и в случаях со многими другими бактериями, еще с 2001 года началось массовое появление антибиотикорезистентных клебсиелл.
В одной из научных работ ученые задались целью узнать, как гены устойчивости к антибиотикам распространены среди штаммов рода Klebsiella. Они обнаружили, что 15 довольно далеких штаммов экспрессировали металло-бета-лактамазу 1 (NDM-1), которая способна разрушать почти все бета-лактамные антибиотики [34]. Бóльшую силу эти факты обретают, если уточнить, что данные для этих бактерий (1777 геномов) получены в период с 2011 по 2015 годы от пациентов, которые находились в разных больницах с разными инфекциями, вызванными клебсиеллами.
Настоящее (влияние на экономику) и будущее
Проблема резистентности бактерий к антибиотикам охватывает сразу несколько сфер человеческой жизни . В первую очередь, это, конечно, экономика. По разным подсчетам, сумма, которую тратит государство на лечение одного пациента с устойчивой к антибиотикам инфекцией, колеблется от $18 500 до $29 000. Эта цифра подсчитана для США, но, пожалуй, ее можно использовать и как средний ориентир по другим странам, чтобы понимать масштаб явления. Такая сумма уходит на одного пациента, но если подсчитать по всем, то оказывается, что суммарно к общему счету, который государство тратит за год на здравоохранение, нужно добавлять $20 000 000 000 [36]. И это помимо $35 000 000 000 социальных расходов. В 2006 году из-за двух наиболее распространенных госпитальных инфекций, в результате которых у людей развивался сепсис и пневмония, умерли 50 тысяч людей. Это обошлось системе здравоохранения США в сумму, превышающую $8 000 000 000.
Ранее мы уже писали про сегодняшнюю ситуацию с антибиотикорезистентностью и о стратегиях по ее предотвращению: «Противостояние с резистентными бактериями: наши поражения, победы и планы на будущее» [37].
Если антибиотики первой и второй линий не работают, то приходится либо увеличивать дозы в надежде на то, что они сработают, либо использовать антибиотики следующей линии. И в том, и в другом случае высока вероятность повышенной токсичности препарата и побочных действий. К тому же, большая доза или новый препарат будут, скорее всего, стоить дороже предыдущего лечения. Это влияет на сумму, которую затрачивают на лечение государство и сам пациент. А также на срок нахождения пациента в больнице или на больничном, число посещений врача и экономические потери от того, что работник не трудится. Большее количество дней на больничном — это не пустые слова. Действительно, пациента с заболеванием, вызванным резистентным микроорганизмом, в среднем приходится лечить 12,7 дней, по сравнению с 6,4 для обычной болезни [30].
Кроме причин, которые непосредственно влияют на экономику — траты на лекарства, на оплату больничных и время нахождения в больнице, — есть еще и немного завуалированные. Это те причины, которые влияют на качество жизни людей, у которых обнаружены антибиотикорезистентные инфекции. Некоторые пациенты — школьники или студенты — не могут в полной мере посещать уроки, и поэтому у них возможны отставание в учебном процессе и психологическая деморализация. У пациентов, которые проходят курсы сильных антибиотиков, из-за побочных эффектов могут развиваться хронические заболевания. Помимо самих пациентов, заболевание морально угнетает их родственников и окружение, а некоторые инфекции настолько опасны, что заболевших приходится содержать в отдельной палате, где они зачастую не могут пообщаться с близкими. Также существование госпитальных инфекций и риск ими заразиться не позволяют расслабиться при прохождении курса лечения. Согласно статистике, около 2 миллионов американцев ежегодно заражаются госпитальными инфекциями, которые в итоге уносят 99 тысяч жизней. Чаще всего это происходит из-за заражения микроорганизмами, устойчивыми к антибиотикам [30]. Важно подчеркнуть, что кроме перечисленных выше и, несомненно, важных экономических потерь, качество жизни у людей тоже сильно страдает.
Прогнозы на будущее разнятся (видео 2). Одни пессимистически указывают на то, что к 2030–2040 годам кумулятивные финансовые потери составят 100 триллионов долларов, что равняется среднегодовому убытку в 3 триллиона долларов. Для сравнения — весь годовой бюджет США лишь на 0,7 триллиона превышает эту цифру [38]. Количество смертей от заболеваний, вызванных резистентными микроорганизмами, по оценке ВОЗ, к 2030–2040 годам приблизится к 11–14 миллионам и превысит смертность от рака.
Видео 2. Лекция Мэрин Маккены на TED-2015 — What do we do when antibiotics don’t work any more?
Неутешительны и перспективы использования антибиотиков в кормах сельскохозяйственных животных (видео 3). В исследовании, опубликованном в журнале PNAS, подсчитали, что в 2010 году во всем мире в кормá было добавлено более 63 000 тонн антибиотиков [38]. И это — только по скромным оценкам. Ожидается, что к 2030 году указанная цифра возрастет на 67%, но, что должно особенно встревожить, она удвоится в Бразилии, Индии, Китае, Южной Африке и России. Понятно, что, раз объемы добавляемых антибиотиков увеличатся, то и расход средств на них тоже увеличится. Существует мнение, что цель добавления их в корм — совсем не улучшение здоровья животных, а ускорение роста. Это позволяет быстро выращивать животных, получать прибыль от продаж и снова выращивать новых. Но при возрастающей антибиотикорезистентности, придется добавлять либо бóльшие объемы антибиотика, либо создавать комбинации из них. В любом из указанных случаев, затраты фермеров и государства, которое нередко их субсидирует, на эти препараты возрастут. При этом продажи сельскохозяйственной продукции могут даже снизиться из-за смертности животных, вызванной отсутствием действенного антибиотика или побочными эффектами нового. А также из-за страха со стороны населения, которое не хочет потреблять продукцию с этим «усиленным» препаратом. Снижение продаж или повышение цены на продукцию может ставить фермеров в бóльшую зависимость от субсидий со стороны государства, заинтересованного в обеспечении населения продуктами первой необходимости, которые как раз и предоставляет фермер. Также, многие сельхозпроизводители из-за вышеуказанных причин могут оказаться на грани банкротства, а, следовательно, это приведет к тому, что на рынке останутся лишь крупные сельскохозяйственные компании. И, как следствие, возникнет монополия крупных компаний-гигантов. Такие процессы негативно отразятся на социально-экономическом положении любого государства.
Видео 3. BBC рассказывает о том, насколько может быть опасным развитие антибиотикорезистентности у сельскохозяйственных животных
По всему миру активно развиваются направления науки, связанные с определением причин генетических заболеваний и их лечения, мы с интересом наблюдаем за тем, что происходит с методами, которые помогут человечеству «избавиться от вредных мутаций и стать здоровыми», как любят упоминать поклонники методов пренатального скрининга, CRISPR-Cas9 и только начинающего развиваться метода генетической модификации эмбрионов [39–41]. Но все это может быть понапрасну, если мы окажемся неспособны противостоять заболеваниям, вызываемым резистентными микроорганизмами. Необходимы разработки, которые позволят преодолеть проблему резистентности, иначе всему миру несдобровать.
Заключение
Меньше века прошло с начала масштабного использования антибиотиков. Вместе с тем, меньше века заняло у нас, чтобы результат этого достиг грандиозных масштабов . Угроза антибиотикорезистентности вышла на глобальный уровень, и было бы глупо отрицать, что именно мы своими же усилиями создали себе такого врага. Сегодня каждый из нас ощущает на себе последствия уже возникшей устойчивости и находящуюся в процессе развития устойчивость, когда получаем от врача выписанные антибиотики, принадлежащие не к первой линии, а второй или даже последней. Сейчас существуют варианты решения этой проблемы, но самих проблем — не меньше. Предпринимаемые нами действия по борьбе с быстро развивающими устойчивость бактериями напоминают гонку. Что будет дальше — покажет время.
Об этой проблеме рассказывает в лекции «Кризис медицины и биологические угрозы» Николай Дурманов, экс-глава «РУСАДА».
И время, действительно, расставляет все по своим местам. Начинают появляться средства, позволяющие улучшить работу уже существующих антибиотиков, научные группы ученых (пока что ученых, но вдруг эта тенденция вновь вернется и к фармкомпаниям) без устали трудятся над созданием и проверкой новых антибиотиков. Обо всем этом можно прочитать и воспрянуть духом во второй статье цикла.
- В диких условиях: как жил последний всеобщий предок LUCA;
- Vanessa M. D’Costa, Christine E. King, Lindsay Kalan, Mariya Morar, Wilson W. L. Sung, et. al.. (2011). Antibiotic resistance is ancient. Nature. 477, 457-461;
- Manisha Deb Mandal, Shyamapada Mandal. (2011). Honey: its medicinal property and antibacterial activity. Asian Pacific Journal of Tropical Biomedicine. 1, 154-160;
- Sultan Ayoub Meo, Saleh Ahmad Al-Asiri, Abdul Latief Mahesar, Mohammad Javed Ansari. (2017). Role of honey in modern medicine. Saudi Journal of Biological Sciences. 24, 975-978;
- Mark L. Nelson, Andrew Dinardo, Jeffery Hochberg, George J. Armelagos. (2010). Brief communication: Mass spectroscopic characterization of tetracycline in the skeletal remains of an ancient population from Sudanese Nubia 350-550 CE. Am. J. Phys. Anthropol.. 143, 151-154;
- A. Coppi, M. Cabinian, D. Mirelman, P. Sinnis. (2006). Antimalarial Activity of Allicin, a Biologically Active Compound from Garlic Cloves. Antimicrobial Agents and Chemotherapy. 50, 1731-1737;
- Balaji Meriga, Ramgopal Mopuri, T. MuraliKrishna. (2012). Insecticidal, antimicrobial and antioxidant activities of bulb extracts of Allium sativum. Asian Pacific Journal of Tropical Medicine. 5, 391-395;
- Mi-Hyang Lee, Hyun Ae Kwon, Dong-Yeul Kwon, Hyun Park, Dong-Hwan Sohn, et. al.. (2006). Antibacterial activity of medicinal herb extracts against Salmonella. International Journal of Food Microbiology. 111, 270-275;
- Anna M Witkowska, Dara K Hickey, Mercedes Alonso-Gomez, Martin Wilkinson. (2013). Evaluation of antimicrobial activities of commercial herb and spice extracts against selected food-borne bacteria. JFR. 2, 37;
- R. Puupponen-Pimia, L. Nohynek, S. Hartmann-Schmidlin, M. Kahkonen, M. Heinonen, et. al.. (2005). Berry phenolics selectively inhibit the growth of intestinal pathogens. J Appl Microbiol. 98, 991-1000;
- Siro Igino Trevisanato. (2007). The ‘Hittite plague’, an epidemic of tularemia and the first record of biological warfare. Medical Hypotheses. 69, 1371-1374;
- Победитель бактерий;
- Эволюция наперегонки, или Почему антибиотики перестают работать;
- Волкова О. (2003). Смерть обходит задворки науки. «Гамма»;
- Ермольева З.В. Биологически активные вещества. М.: «Знание», 1966. — 32 с.;
- Saswati Sengupta, Madhab K. Chattopadhyay, Hans-Peter Grossart. (2013). The multifaceted roles of antibiotics and antibiotic resistance in nature. Front. Microbiol.. 4;
- Abraham E.P. and Chain E. (1940). An enzyme from bacteria able to destroy penicillin. Nature. 3713, 837;
- Walter Sneader. (2001) History of Sulfonamides;
- Главный «почвенник» медицины: Зельман Ваксман;
- Ремиш А. (2016). Битва за выживание. Econet;
- Chih-Chia Su, Linxiang Yin, Nitin Kumar, Lei Dai, Abhijith Radhakrishnan, et. al.. (2017). Structures and transport dynamics of a Campylobacter jejuni multidrug efflux pump. Nat Commun. 8;
- Nitin Kumar, Chih-Chia Su, Tsung-Han Chou, Abhijith Radhakrishnan, Jared A. Delmar, et. al.. (2017). Crystal structures of theBurkholderia multivoranshopanoid transporter HpnN. Proc Natl Acad Sci USA. 114, 6557-6562;
- A. P. Johnson. (2011). Methicillin-resistant Staphylococcus aureus: the European landscape. Journal of Antimicrobial Chemotherapy. 66, iv43-iv48;
- G. V. Doern, K. P. Heilmann, H. K. Huynh, P. R. Rhomberg, S. L. Coffman, A. B. Brueggemann. (2001). Antimicrobial Resistance among Clinical Isolates of Streptococcus pneumoniae in the United States during 1999-2000, Including a Comparison of Resistance Rates since 1994-1995. Antimicrobial Agents and Chemotherapy. 45, 1721-1729;
- Rayner E. (2015). AncientBiotics — a medieval remedy for modern day superbugs? The University of Nottingham;
- Macdonald F. (2015). 1,000-year-old onion and garlic remedy kills antibiotic-resistant bugs. ScienceAlert;
- Керман А. (2017). ВОЗ обеспокоена неизлечимой гонореей. «XXII ВЕК»;
- Gian Maria Rossolini, Fabio Arena, Patrizia Pecile, Simona Pollini. (2014). Update on the antibiotic resistance crisis. Current Opinion in Pharmacology. 18, 56-60;
- Ventola C.L. (2015). The antibiotic resistance crisis. Part 1: causes and threats. P.T. 40, 277–283;
- Zhabiz Golkar, Omar Bagasra, Donald Gene Pace. (2014). Bacteriophage therapy: a potential solution for the antibiotic resistance crisis. J Infect Dev Ctries. 8;
- Michael Gross. (2013). Antibiotics in crisis. Current Biology. 23, R1063-R1065;
- Березняков И.Г. (2009). Приверженность к приему лекарственных средств и пути ее повышения при бактериальных инфекциях. Болезни и антибиотики. 2;
- S. Karuthu, E. A. Blumberg. (2012). Common Infections in Kidney Transplant Recipients. Clinical Journal of the American Society of Nephrology. 7, 2058-2070;
- S. Wesley Long, Randall J. Olsen, Todd N. Eagar, Stephen B. Beres, Picheng Zhao, et. al.. (2017).
Population Genomic Analysis of 1,777 Extended-Spectrum Beta-Lactamase-Producing
Klebsiella pneumoniae
Isolates, Houston, Texas: Unexpected Abundance of Clonal Group 307
. mBio. 8, e00489-17; - Martin J Llewelyn, Jennifer M Fitzpatrick, Elizabeth Darwin, SarahTonkin-Crine, Cliff Gorton, et. al.. (2017). The antibiotic course has had its day. BMJ. j3418;
- Margaret A. Riley, Sandra M. Robinson, Christopher M. Roy, Morgan Dennis, Vivian Liu, Robert L. Dorit. (2012). Resistance is futile: the bacteriocin model for addressing the antibiotic resistance challenge. Biochm. Soc. Trans.. 40, 1438-1442;
- Противостояние с резистентными бактериями: наши поражения, победы и планы на будущее;
- Thomas P. Van Boeckel, Charles Brower, Marius Gilbert, Bryan T. Grenfell, Simon A. Levin, et. al.. (2015). Global trends in antimicrobial use in food animals. Proc Natl Acad Sci USA. 112, 5649-5654;
- CRISPR-эпопея и ее герои;
- Просто о сложном: CRISPR/Cas;
- От слов к делу: технологию CRISPR-Cas впервые применили для лечения онкозаболеваний.
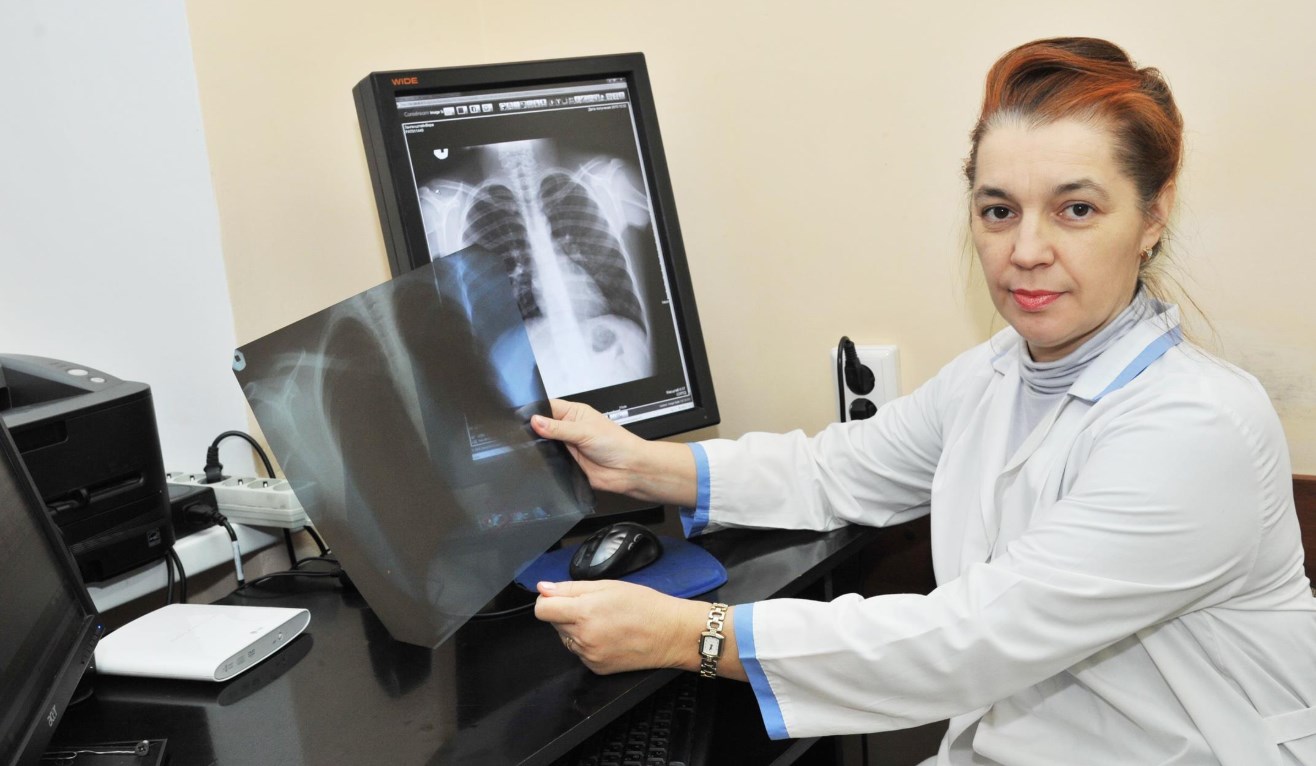
Антибиотики – это вещества биологического или полусинтетического происхождения. Применяются в лечебной практике для борьбы с болезнетворными микробами, вирусами. До появления этих медпрепаратов статус неизлечимых болезней был у брюшного тифа, дизентерии, пневмонии, туберкулеза. Сегодня лечение заболеваний инфекционного характера возможно с применением 1-6 поколения антибиотиков.
На этот момент фармакологическая индустрия выпускает более 2000 разновидностей лекарственных средств подобного типа. Медики описали действие около 600 позиций, а во врачебной практике используются порядка 120-160 препаратов.
Важно! При любом заболевании принимать антибиотики рекомендуется после консультации с врачом. В противном случае может развиться антибиотикорезистентность (снижение чувствительности патогенных микроорганизмов к антибактериальным средствам).
Классификация антибиотиков
Все антибактериальные средства можно разделить на 5 категорий по характеристикам и спектру применения. Рассмотрим эту классификацию подробнее:
Механизм воздействия:
- Бактерицидные – активные вещества препаратов полностью уничтожают бактерии, вирусы. После приема таких сильных лекарств вся болезнетворная микрофлора в организме человека погибает.
- Бактериостатические – подавляют рост или распространение вирусов. Таким образом, клетки остаются «живыми», не образуя патогенной флоры.
Спектр действия
Различают антибактериальные средства:
- Широкого диапазона воздействия – их назначают при болезнях инфекционного характера с невыясненной причиной недомогания. Это бактерицидные медпрепараты, поскольку уничтожают всю патогенную флору.
- Узкого диапазона воздействия – уничтожают грамположительные бактерии (энтерококки, листерии). После их приема погибают также грамотрицательные возбудители инфекционных болезней: кишечной палочки, сальмонеллы, протей и т.д. К этой группе относятся также противотуберкулезные, противоопухолевые, противогрибковые средства.
По составу
Антибактериальные препараты делят на 6 групп:
- Пенициллины – первые антимикробные препараты, полученные ещё в 1928 году из биологического вещества (грибы Penicillium). Долго оставались самым популярным медикаментом для лечения инфекционных болезней.
- Цефалоспорины – относятся к группе самых сильных противомикробных средств обширного диапазона применения. Полностью уничтожают патогенную флору, хорошо переносятся человеком.
- Макролиды – это название группы антимикробных средств узкого диапазона. Не уничтожают больную клетку, а только останавливают её рост. В эту категорию входят такие препараты: эритромицин, спирамицин, азитромицин.
- Тетрациклины – хорошие препараты для лечения инфекционных заболеваний дыхательных, а также мочевыводящих путей.
- Фторхинолоны – противомикробные средства обширного диапазона воздействия. Уничтожают полностью патогенные микроорганизмы. В продаже можно встретить медпрепараты 1-2 поколения. Обычно врачи их приписывают для борьбы с синегнойной палочкой.
- Аминогликозиды – противомикробные лекарства с большой областью применения. Популярные лекарства этой группы – стрептомицин (терапия туберкулеза, чумы) и гентамицин – используются как мазь, глазные капли, инъекции при офтальмологических инфекциях.
Поколения препаратов. У передовых антимикробных препаратов насчитывается уже шесть генераций. Например, пенициллин был первым средством природного происхождения, тогда как третья или шестая генерация – это уже улучшенная версия, которая включает в состав сильнейшие ингибиторы. Зависимость прямая: чем новее генерация, тем эффективнее воздействие препаратов на патогенную микрофлору.
По способу приема. Пероральные – принимают через рот. Это различные сиропы, таблетки, растворимые капсулы, суспензии. Парентеральные – вводятся внутривенно или внутримышечно. Они быстрее дают эффект, чем пероральные лекарства. Ректальные препараты вводятся в прямую кишку.
Важно! Принимать антибиотики допускается только после консультации с врачом, иначе разовьется антибиотикорезистентность.
Антибактериальные средства нового поколения
Отличие последних генераций антибиотиков от их ранних версий в более совершенной формуле действующего вещества. Активные компоненты точечно устраняют только патологические реакции в клетке. Например, кишечные антибиотики нового поколения не нарушают микрофлору ЖКТ. При этом они борются с целой «армией» возбудителей инфекций.
Новейшие антибактериальные препараты делятся на пять групп:
- Тетрациклиновая – тетрациклин.
- Аминогликозиды – стрептомицин.
- Пенициллиновый ряд – амоксициллин и другие.
- Амфениколы – хлорамфеникол.
- Карбапенемовая группа – меропенем, имипенем, инваз.
Рассмотрим несколько известных противомикробных средств импортного и российского производства.
Амоксициллин – импортный противомикробный препарат из группы пенициллинов. Используется во врачебной практике для лечения бактериальной инфекции. Эффективен при кишечных инфекциях, гайморите, ангине, болезни Лайма, дизентерии, сепсисе.
Авелокс – медпрепарат последней генерации из группы фторхинолонов. Отличается сильнейшим воздействием на бактериальные и атипичные возбудители. Не вредит почкам и ЖКТ. Используется при острых, хронических заболеваниях.
Цефалоспорины – антибиотики третьего поколения. К этой группе относят Цефтибутен, Цефтриаксон и другие. Используются для лечения пиелонефрита, пневмонии. В целом это безопасные средства с малым количеством побочных действий. Однако их нужно принимать только после консультации с врачом. Медпрепаратов много, а какой именно выбрать – порекомендует специалист.
Дорипрекс – импортный противомикробный препарат синтетического происхождения. Показал хорошие результаты при лечении пневмонии, запущенных интраабдоминальных инфекций, пиелонефритах.
Инваз – антибактериальное средство из группы карбапенемов. Выпускается в ампулах для парентерального способа применения. Показывает быстрый эффект при лечении бактериальных расстройств кожи, мягких тканей, инфекциях мочевыводящих путей, пневмонии, септицемиях.
Аугметин – полусинтетический пенициллин третьей генерации с добавлением усиливающих ингибиторов. Педиатрами признается лучшим комплексным медпрепаратом для лечения детских гайморита, бронхита, тонзиллита и других инфекций дыхательных путей.
Цефамандол – антибактериальное средство российского производства. Относится к группе цефалоспоринов третьего поколения. Используется для лечения кишечных инфекций, возбудителей инфекций половых органов. Как противомикробное средство обширного диапазона воздействия применяется при простудных заболеваниях.
Лучшие антибактериальные препараты широкого диапазона действия
Противомикробные средства новой генерации обычно синтезируют из природного сырья и стабилизируют в лабораториях. Это помогает усилить эффект лекарства на патогенную микрофлору.
Какие препараты самые сильные? Врачи относят к таким антибактериальные средства широкого спектра воздействия. Приведем ниже краткий список препаратов по названиям:
- АМОКСИКЛАВ – относится к группе аминопенициллинов. Действует мягко, используется для лечения инфекционных заболеваний. С осторожностью и только после консультации с врачом препарат можно применять при беременности, а также в периоды кормления грудью. Выпускается в таблетках или в сыпучей форме для перорального приема, а также в порошках для инъекций.
- СУМАМЕД – популярный противомикробный препарат для лечения инфекций ЖКТ, мочеполовой системы, болезней дыхательный путей – ангины, бронхита, пневмонии. Воздействует на печень и почки, поэтому его не приписывают пациентам с повышенной чувствительностью к макролидам.
- ЦЕФОПЕРАЗОН – относится к группе цефалоспоринов. Приписывается врачами для лечения инфекций мочевыводящих путей, простатита, кожных расстройств, болезней дыхательных путей. Хороший препарат для восстановления после гинекологических, ортопедических и абдоминальных операций. Выпускается в форме для парентерального приема – инъекции.
- ЮНИДОКС СОЛЮТАБ – тетрациклин последней генерации. Применяется для обширного лечения инфекций ЖКТ, простудных заболеваний, простатита. Действует мягко, не вызывая дисбактериоза.
- ЛИНКОМИЦИН – средство, которое назначают для лечения остеомиелита, сепсиса, стафилококковых инфекций. Оказывает сильнейшее воздействие на патогенные клетки, поэтому имеет длинный ряд побочных эффектов. Среди них – гипотония, слабость, головокружение. Нельзя применять при беременности, а также пациентам с печеночно-почечной недостаточностью.
- РУЛИД – макролид четвертой генерации. Основное вещество – рокситромицин. Приписывают при урогенитальных инфекциях, болезнях ЖКТ и верхних дыхательных путей. Выпускается в таблетках.
- ЦЕФИКСИМ – по названию это средство из группы цефалоспоринов. Оказывает бактерицидное воздействие на патогенные клетки. Помогает при инфекциях ЖКТ, простатите, также лечит простудные заболевания. Достаточно токсичен, поэтому его нельзя принимать при проблемах с почками или печенью.
- ЦЕФОТАКСИМ – последняя группа цефалоспоринов. Медпрепарат показан для лечения гинекологических, урологических, простудных заболеваний. Отлично справляется с воспалительными процессами, подавляет патогенную микрофлору.
Резюме
Мы рассмотрели российские и импортные антибиотики широкого спектра действия, кратко описали классификацию препаратов. Ответим на вопрос: какие антибактериальные средства выбрать?
Важно понимать, противомикробные лекарства для обширного применения обладают токсичностью, поэтому негативно влияют на микрофлору. Кроме того, бактерии мутируют, а значит препараты теряют свою эффективность. Поэтому антибактериальные средства с новейшей структурой будут в приоритете, чем их ранние аналоги.
Самолечение антибиотиками опасно для здоровья. При инфекционном заболевании первым делом нужно обратиться к врачу. Специалист установит причину болезни и назначит эффективные антибактериальные средства. Самолечение «наугад» приводит к развитию антибиотикорезистентности.
Назад к списку
Антибиотики – сильные препараты для лечения бактериальных инфекций, но их бесконтрольный прием может негативно сказаться на здоровье.
В каких случаях врачи назначают антибиотики? Как избежать ошибок при применении антибиотиков? Какие есть риски при неправильном применении этой группы препаратов? – На эти и другие вопросы ответила Татьяна Бирюкова, врач-терапевт высшей категории «ИНВИТРО-Урал».
При каких заболеваниях назначают лечение антибиотиками? Как они действуют на организм (польза/вред)? Как борются с заболеваниями?
Антибиотики применяются для лечения заболеваний, вызванных бактериями. Именно вызванных бактериями, на вирусы они не действуют. Польза антибиотиков состоит в том, что они успешно борются с тяжелыми бактериальными инфекциями, с которыми иммунная система организма человека самостоятельно справиться не может. Например, с такими заболеваниями, как пневмония, пиелонефрит, ангина, сифилис, туберкулез и многие другие. До создания антибиотиков была высокая смертность от инфекционных заболеваний.
Антибиотик может бороться с микроорганизмами разными путями, подавляя их размножение или вызывая гибель бактерии. Оба механизма эффективны и приводят к выздоровлению человека.
Как и любое другое лекарство, антибиотики могут вызывать разные побочные эффекты в зависимости от препарата, его состава. К общим побочным эффектам для всех АБ относятся риск развития аллергических реакций, дисбактериоза и АБ-ассоциированных колитов.
Почему не стоит пить антибиотики без назначения врача? Какие есть риски для здоровья?
Человеку самому сложно или невозможно разобраться что стало причиной заболевания – вирусы, бактерии, нарушения в иммунной системе или развитие аутоиммунных процессов.
В такой ситуации есть риск получить побочные эффекты и осложнения от неправильного самостоятельного лечения и затянуть с началом необходимой терапии. Например, человек заболел гриппом и сразу начал пить АБ. А в такой ситуации он не поможет, так как на вирус не действует, да и еще провоцирует иммуносупрессию – угнетенние иммунитета, что неблагоприятно скажется на течении заболевания. В то же время к вирусной инфекции может присоединяться бактериальная инфекция, и вот здесь уже нужен АБ, но заранее его принимать бесполезно. АБ не проводит профилактику, он работает только когда есть бактерия, присоединяясь к ней и убивая ее.
В каких случаях назначают лабораторные исследования для подбора антибиотиков?
При любом заболевании, вызванном бактериями лучше определять их чувствительность к АБ. Крайне необходимо сдать анализы в следующих случаях:
- в случае тяжелого течения инфекционного заболевания;
- при повторном проведении АБ- терапии через небольшой интервал времени (менее 3-х месяцев);
- при наличии иммунодефицитных состояний у человека;
- при тяжелой сопутствующей патологии;
- при вероятной резистентности бактерий, например, в случае частых госпитализаций в стационар, где есть «больничная флора», которая часто устойчива к АБ.
Почему важно пропить весь курс антибиотиков, а не бросить после того, как уйдут симптомы?
Только при проведении полного курса АБ происходит гибель бактерий. Если же курс прервать, то за это время бактерии только ослабевают под действием АБ, но не гибнут. Кроме того, незавершенные курсы АБ-терапии являются одной из причин развития резистентности (устойчивости) бактерий к АБ.
Когда уходят симптомы — это лишь признак того, что лечение подобрано верно и АБ эффективен. Длительность АБ зависит от выбранного АБ-препарата и заболевания пациента.
Нужно ли пить дополнительно какие-то препараты, чтобы восстановить организм во время или после курса антибиотиков?
Правильным будет во время всего курса АБ-терапии принимать пробиотик для профилактики развития дисбактериоза и АБ-ассоциированного колита. Курс приема пробиотика может быть продлен и после завершения приема АБ. Длительность курса определяет врач. Как правило, курс приема соответствует схеме, указанной в инструкции к пробиотику.
Хочется обратить внимание и на прямую связь нашего иммунитета с образом жизни, так как лекарства могут исправить многое, но не всё. Независимо от возраста организму полезно сбалансированное, регулярное питание, движение, соблюдение режима дня, положительные эмоции и достаточный сон.
Почему при приеме антибиотиков нельзя алкоголь?
Одновременный прием АБ и алкоголя влияет на «переработку» в организме и АБ, и алкоголя, что может привести к замедленному выведению и накоплению в организме АБ или алкоголя, а значит спровоцировать токсическую реакцию. Чаще всего страдает печень, почки, сердечно-сосудистая система.
Кроме того, алкоголь может оказывать разрушающее действие на сам антибиотик, препятствовать его связыванию с бактериями или ускорить выведение АБ из организма, снижая эффективность лечения.
Если человек достаточно долгое время принимает антибиотики (например, лечит не связанные между собой патологии одну за другой) – может ли повлиять на здоровье?
К сожалению, может повлиять. В такой ситуации выше риск развития дисбактериоза, антибиотик-ассоциированных колитов (диарея), лекарственных гепатитов, аллергических реакций, резистентности к антибиотик- терапии и других осложнений.
Что такое антибиотикорезистентность? Почему она развивается?
Антибиотикорезистентность – это устойчивость бактерий к антибиотику. То есть антибиотик становится знакомым, привычным для бактерии и неэффективным для лечения.
Причин несколько:
- широкое применение АБ-препаратов;
- прием АБ без показаний;
- нарушение схем приема АБ;
- содержание АБ в пищевых продуктах.
Бактерии – простейшие организмы, но, как и все живое, стремящиеся сохранить свою жизнь. Поэтому они пытаются приспособиться к АБ, вырабатывают вещества, которые защищают их от действия АБ, бывают ситуации, когда бактерия настолько адаптируется к АБ, что начинает его использовать в качестве питательной среды для себя.
Все эти причины приводят к появлению бактерий устойчивых к определенным АБ или даже ко всем АБ, так в мире сейчас появились супербактерии, которые вызывают появление трудноизлечимых смертельно опасных инфекционных заболеваний. Эта проблема актуальна для всего мира.
Необходимой мерой для предупреждения АБ-резистентности является прием АБ только по показаниям врачам и полное соблюдение схемы лечения, показанной для конкретной клинической ситуации.
Важно соблюдать все условия приема АБ, которые можно прочитать в инструкции к лекарству – связь с приемом пищи, интервал между приемом АБ в случае его приема несколько раз в день.
В каких случаях можно обойтись без лечения антибиотиками?
При легком течении бактериальной инфекции можно обойтись без АБ-терапии. Врач в этом случае назначает терапию и контролирует ее эффективность. Например, в лор-практике синуситы при нетяжелом лечении успешно лечатся лор-врачом местными видами терапии.
Влияние антибиотиков на организм
Антибиотики и их влияние на здоровье
Хотя лечение антибиотиками часто сопровождается целым рядом осложнений, после которых не так-то просто восстановить организм, эти лекарства продолжают активно применяться и назначаться пациентам, в том числе детям и беременным женщинам.
Что такое антибиотики
Антибиотики – это особые вещества биологического происхождения, способные подавлять рост вирусов, микробов и микроорганизмов или полностью уничтожать их. Специфичность действия является основной особенностью антибиотиков. То есть, каждый конкретный вид патогенных микроорганизмов является восприимчивым не к каждому типу антибиотиков. Именно эта особенность легла в основу классификации современных антибиотиков на препараты узкого спектра действия (подавляют жизнедеятельность микробов одного вида) и широкого спектра действия (уничтожают различные виды микроорганизмов).
Антибиотики призваны помочь человеку побороть инфекционное заболевание, но при этом крайне важно не нанести дополнительного вреда здоровью. Чтобы не пришлось столкнуться с серьезными осложнениями, недопустим бесконтрольный прием подобных лекарств – любе препараты должны назначаться врачом и приниматься строго под его контролем.
Негативное влияние антибиотиков на организм
Прежде чем перечислить возможные негативные последствия от приема антибиотиков, необходимо отметить, что при ряде заболеваний лечение антибактериальными препаратами является крайней необходимостью. Речь идет о таких патологиях как пневмония, сепсис, гнойная ангина и т.д. И если непродолжительное применение антибиотиков способно дать очень хороший эффект, то слишком длительное их использование способно привести к тяжелым побочным эффектам:
- Происходит подавление не только патогенной, но и полезной микрофлоры в организме. Это приводит к тому, что в вашем организме создается своеобразная «безжизненная среда», в которой могут существовать только микроорганизмы с выработанной устойчивостью.
- Происходит нарушение клеточного дыхания, а значит, доступ кислорода к тканям значительно ограничивается, то есть ваш организм как бы переходит в анаэробное состояние.
- Негативно влияют антибиотики и на печень, забивая желчные проходы этого органа. Причем отрицательное влияние это намного сильнее, чем от регулярного употрeбления спиртного.
- Стремительно истощаются и буферные системы печени, основное предназначение которых состоит в компенсации токсических воздействий. Постепенно печень кардинально меняет свои функции и вместо очищения она загрязняет наш организм. Для того чтобы избежать этого негативного последствия, в ряде случаев наши врачи назначают в дополнение к антибиотикам препараты для поддержки нормальной работы печени.
- Длительный прием антибиотиков в прямом смысле слова «выключает» нашу иммунную систему.
Это лишь небольшая часть тех вредных воздействий, которые антибиотики могут оказывать на человеческий организм. В зависимости от конкретного типа препарата этот список может пополняться. Именно из-за столь обширного списка тяжелых побочных эффектов специалисты нашей клиники стараются прибегать к лечению антибиотиками лишь в самых крайних случаях, когда остальные средства оказываются неэффективными.
Антибиотики и микрофлора
Вы уже знаете, что в основе воздействия антибиотиков лежит подавление и уничтожение микрофлоры. Наш организм в совокупности с населяющей его микрофлорой формируют стабильный гомеостаз. Таким образом, качество нашей жизнедеятельности регулируется именно балансом всех протекающих процессов. Любой антибиотик является ингибитором, подавляющим химические реакции, в том числе и полезных микробов, что негативно влияет и на гомеостаз.
Простыми словами, антибиотики внутри нас обеспечивают своеобразную временную стерильность. В такой среде ни один микроорганизм кроме самих патогенных микробов существовать не может, а это чревато развитием самых различных патологий. Совершенно ошибочно полагать, что микрофлора способна быстро восстановиться после такого воздействия. Именно поэтому наши врачи, назначая пациентам антибиотики, выписывают и препараты, поддерживающие микрофлору кишечника.
Антибиотики при беременности
Применение антибиотиков в период беременности – это тема довольно сложная и спopная. Вы, конечно, знаете, что в этот период нежелателен прием вообще любых лекарственных препаратов, но что делать, если организму пришлось столкнуться с серьезной инфекцией, угрожающей плоду? Специалисты нашей клиники никогда не назначают антибактериальное лечение беременным без серьезных на то показаний. Ими могут являться пoлoвые инфекции, пиелонефрит, пневмония и т.д.
При назначении препаратов обязательно учитывается срок беременности. Крайне нежелательно применять антибиотики в первом триместре, когда происходит формирование жизненно важных органов плода. В этом случае антибактериальные препараты способны повреждать функции и органы ребенка, вызывая врожденные патологии. Если лечение матери все же необходимо, наши врачи обеспечивают строжайший контроль над процессом терапии, чтобы при возникновении даже малейших осложнений отменить препарат.
Если вам пришлось пройти курс лечения антибиотиками еще до беременности, но вы планируете зачатие, то его лучше отложить на два-три месяца. Однако если беременность наступила незапланированно, не переживайте: антибиотики, прием которых осуществлялся до задержки мecячных, вряд ли смогут негативно повлиять на здоровье вашего ребенка.
Как принимать антибиотики без вреда для здоровья
Основное условие, соблюдение которого необходимо для эффективного лечения антибиотиками с минимальным вредом для организма, – это прием препаратов строго по назначению врача с соблюдением дозировки, времени приема лекарств и длительности курса лечения. Если вы принимаете какие-то другие лекарства, обязательно сообщите об это нашему врачу, так как прием некоторых препаратов может быть несовместим с антибиотиками. Также на время курса лечения следует воздержать от употрeбления спиртного.
Необходимо срочно обратиться к врачу, если на фоне приема антибиотиков у вас обнаружились аллергические реакции, а также если улучшение самочувствия не наступает, а к имеющимся клиническим проявлениям добавились новые патологические симптомы.
Итак, как вы видите, антибиотики являются довольно «коварными» лекарствами, без которых, с одной стороны, обойтись нельзя, но с другой – после лечения ими восстановиться бывает довольно сложно. Если возникла крайняя необходимость, и наш врач выписал вам тот или иной антибиотик, строго соблюдайте все предписания и не прекращайте курс лечения даже при быстром наступлении улучшений.
Влияние антибиотиков на организм человека
С открытием пенициллина в 1928 году настала новая эпоха в жизни людей, эпоха антибиотиков. Мало кто задумывается над тем, что до этого открытия в течение тысячелетий главной опасностью для человека являлись именно инфекционные болезни, которые периодически принимали масштаб эпидемий, выкашивая целые регионы. Но и без эпидемий cмepтность от инфекций была чрезвычайно высока, и низкая продолжительность жизни, когда 30-летний человек считался пожилым, была обусловлена именно этой причиной.
Антибиотики перевернули мир, изменили жизнь если не больше, чем изобретение электричества, то уж точно не меньше. Почему же мы относимся к ним настороженно? Причина в неоднозначном влиянии этих лекарств на организм. Попробуем разобраться, каково же это влияние, и чем на самом деле стали антибиотики для людей, спасением или проклятием.
Препараты против жизни?
«Anti bios» в переводе с латинского означает «против жизни», получается, антибиотики – лекарства против жизни. Леденящее кровь определение, не правда ли? На самом деле, на счету антибиотиков миллионы спасенных жизней. Научное название антибиотиков – антибактериальные препараты, что более точно соответствует их функции. Таким образом, действие антибиотиков направлено не против человека, а против микроорганизмов, которые проникают в его организм.
Опасность в том, что большинство антибиотиков влияют не на одного возбудителя той или иной болезни, а на целые группы микробов, где есть не только болезнетворные бактерии, но и те, что необходимы для нормального функционирования организма.
Известно, что в кишечнике человека содержится около 2 кг микробов – огромное количество главным образом бактерий, без которых нормальное функционирование кишечника невозможно. Полезные бактерии присутствуют также на коже, в полости рта и влагалище – во всех местах, где может происходить контакт организма с чужеродной для него средой. Разные группы бактерий сосуществуют в балансе друг с другом и с иными микроорганизмами, в частности, с грибками. Нарушение баланса приводит к чрезмерному росту антагонистов, тех же грибков. Так развивается дисбактериоз, или дисбаланс микроорганизмов в теле человека.
Дисбактериоз это одно из самых распространенных негативных последствий приема антибиотиков. Частным его проявлением являются грибковые инфекции, яркий представитель которых – всем известная молочница. Вот почему, назначая антибиотики, врач обычно назначает и препараты, способствующие восстановлению микрофлоры. Однако принимать такие препараты нужно не во время антибиотикотерапии, а после нее.
Понятно, что чем более мощный препарат принимается и чем шире его спектр действия, тем больше бактерий погибнет. Вот почему желательно применять антибиотики широкого спектра действия только в случае крайней необходимости, а во всех иных ситуациях подбирать препарат узкого спектра действия, оказывающий прицельное влияние лишь на небольшие, нужные группы бактерий. Это является важной мерой профилактики дисбактериоза при проведении антибиотикотерапии.
Читать еще: Как распознать и как выглядит аллергия на коже у взрослых: фото первых признаков, вероятные аллергены и особенности терапии
Вредное воздействие полезных лекарств
Давно установлено, что безвредных лекарств не существует в природе. Даже самый безобидный препарат при неправильном применении вызывает нежелательные эффекты, что уж говорить о таких мощных лекарствах, как антибиотики.
Следует понимать, что побочные эффекты это возможное, но необязательное последствие приема антибактериальных средств. Если препарат прошел испытания и принят в клиническую практику, это значит, было однозначно и убедительно доказано, что его польза для большинства людей значительно превышает возможный вред. Тем не менее, все люди имеют особенности, реакция каждого организма на лекарство обусловливается сотнями факторов, и есть некоторое количество людей, чья реакция на препарат по той или иной причине оказалась скорее негативной.
Возможные негативные реакции всегда перечисляются в списке побочных эффектов любого лекарства. У антибиотиков способность вызывать побочные действия выражена достаточно сильно, поскольку они мощно влияют на организм.
Остановимся на основных нежелательных последствиях их приема:
- Аллергические реакции. Проявляться они могут по-разному, чаще всего это кожная сыпь и зуд. Аллергию могут вызывать любые антибиотики, но наиболее часто это цефалоспорины, бета-лактаны и пенициллины;
- Токсическое воздействие. Особенно уязвима в этом отношении печень, выполняющая в организме функцию очистки крови от ядов, и почки, через которые происходит выведение токсинов из организма. Гепатотоксическим действием обладают, в частности, антибиотики тетрациклинового ряда, а нефротоксическим – аминогликозиды, полимексины и некоторые из цефалоспоринов. Помимо этого, аминогликозиды могут вызвать необратимое поражение слухового нерва, что приводит к глухоте. Поражающим нервные структуры действием также обладают фторхинолоны и антибактериальные средства нитрофуранового ряда. Левомицетин оказывает токсическое влияние на кровь и на эмбрион. Негативным влиянием на процесс кроветворения известны антибиотики группы амфениколов, цефалоспорины и некоторые виды пенициллина;
- Подавление иммунитета. Иммунитет это защитные силы организма, его «оборона», оберегающая организм от вторжения болезнетворных агентов. Подавление иммунитета ослабляет естественную защиту организма, вот почему антибиотикотерапия не должна быть чрезмерно длительной. В той или иной степени иммунитет подавляет большинство антибактериальных препаратов, наиболее негативно в этом отношении действие тетрациклинов и того же левомицетина.
Таким образом, становится понятным, почему врачи настаивают на том, чтобы никогда и ни при каких условиях пациенты не занимались самолечением, тем более самолечением антибиотиками. При бездумном применении, при игнорировании имеющихся особенностей организма, лекарство может оказаться хуже болезни. Означает ли это, что антибиотики вредны? Разумеется, нет. Ответ лучше всего проиллюстрировать примером ножа: мало какой инструмент был и остается столь нужным и полезным человеку, однако при неправильном применении нож может стать орудием убийства.
Когда антибиотики вредны
Итак, антибиотики скорее полезны для человечества, хотя могут принести вред при определенных условиях. Однако есть состояния, когда прием антибиотиков однозначно не нужен. Это следующие патологии:
- Вирусные заболевания, включая грипп, которые врачи объединяют названием ОРВИ, а люди, не связанные с медициной, называют простудой. Антибактериальные препараты не действуют на вирусы, мало того, они снижают иммунитет, который является основным противовирусным инструментом;
- Диарея. Как мы выяснили ранее, прием антибиотиков может привести к дисбактериозу, одним из проявлений которого является именно диарея. При кишечных расстройствах антибиотики если и принимаются, то только по назначению врача после точного выявления возбудителя;
- Повышенная температура, головная боль, кашель. Вопреки расхожему мнению, антибиотик не является ни жаропонижающим средством, ни обезболивающим, ни противокашлевым. Высокая температура, кашель, головная, мышечная или суставная боль это лишь симптомы, присущие множеству заболеваний. Если они вызваны не бактериями, прием антибиотиков совершенно бесполезен, а с учетом побочных действий скорее вреден.
Подводя итог нужно сказать, что антибиотики – мощное и действенное лекарство, чье влияние на организм полностью зависит от того, насколько правильно оно используется.
Инфекции человека
- Бактериальные инфекции (41)
- Биохимия (5)
- Вирусные гепатиты (12)
- Вирусные инфекции (43)
- ВИЧ-СПИД (28)
- Диагностика (30)
- Зооантропонозные инфекции (19)
- Иммунитет (16)
- Инфекционные заболевания кожи (33)
- Лечение (38)
- Общие знания об инфекциях (36)
- Паразитарные заболевания (8)
- Правильное питание (41)
- Профилактика (23)
- Разное (3)
- Сепсис (7)
- Стандарты медицинской помощи (26)
10 последствий вреда антибиотиков
Всем привет, с вами Ольга Рышкова. Врачи назначают антибиотики для лечения заболеваний, вызванных бактериями, такими как некоторые инфекции дыхательных путей, инфекции кожи и инфицированных ран. Эти препараты блокируют жизненно важные процессы у бактерий, либо убивают их, либо останавливают их размножение. Это помогает нашей естественной иммунной системе бороться с инфекцией.
Различные антибиотики работают по-разному в отношении бактерий. Например, пенициллин разрушает клеточные стенки бактерий, а эритромицин останавливает строительство белка в бактериях.
Надлежащее применение антибиотиков имеет важное значение для своевременного лечения различных инфекций, однако они могут оказывать побочные эффекты, которые вызывают другие временные проблемы со здоровьем. Некоторые из них могут даже вызывать более серьезные заболевания. Какой вред оказывают антибиотики (т.е. антибактериальные препараты) на организм человека?
Вот 10 последствий вредного воздействия антибиотиков на детей и взрослых.
1. Диарея и запор.
Это два частых побочных эффекта применения антибиотиков. Антибактериальные препараты не разбираются, какие бактерии плохие, какие хорошие и нарушают баланс кишечной флоры, убивая нужные микроорганизмы наряду с инфекционными. Это приводит к антибиотик-ассоциированной диарее или запору. Среди них цефалоспорины, клиндамицин, пенициллин и фторхинолоны.
Использование пробиотиков эффективно в профилактике и лечении антибиотик-ассоциированной диареи и запора. Чтобы предотвратить или лечить этот побочный эффект, добавьте пробиотические йогурт, кефир, квашеную капусту в свой рацион.
2. Тошнота и рвота.
Принимая антибиотики, такие как пенициллин и метронидазол, многие люди испытывают тошноту и рвоту. Эти симптомы возникают, когда антибактериальные препараты убивают некоторые из полезных бактерий, живущих в вашем кишечнике. Возникает вздутие живота, тошнота и рвота, которые обычно слабо выражены и преходящи. В этом случае вы можете съесть пробиотический йогурт и выпить имбирный чай.
3. Вагинальные грибковые инфекции.
Грибок кандида и другие микроорганизмы, живущие во влагалище женщины, безвредны, если естественным образом сбалансированы. Антибиотики, такие как клиндамицин и тетрациклин, используемые для лечения инфекций, меняют естественный баланс в сторону увеличения грибков, убивая полезные бактерии. Это и приводит к развитию грибковой инфекции. Её симптомы — обильные, белые выделения из влагалища, жжение и зуд. Для лечения врач назначает противогрибковые препараты.
4. Аллергические реакции.
У некоторых людей есть аллергия на антибиотики, такие как пенициллин и цефалоспорины. Аллергические реакции могут включать такие симптомы, как крапивница, кожная сыпь, зуд, отёки, одышка, хрипы, насморк, лихорадка и анафилаксии.
Кроме того, исследования показывают связь между вредным воздействием антибиотиков на плод при беременности или в детстве и последующей астмой. Сведите к минимуму использование антибиотиков и держитесь от них подальше от тех, на которые у вас аллергия. Сообщайте о нeблагоприятных реакциях врачу, чтобы он заменил препарат.
5. Ослабление иммунитета.
Дружественные нам бактерии в желудочно-кишечном тракте формируют значительную часть иммунитета организма. Антибактериальные препараты без разбора убивают полезные и вредные бактерии и их длительное применение существенно снижает эффективность иммунной системы, тем самым увеличивая риск развития вторичных бактериальных инфекций. Лучше включите в свой рацион продукты с антибиотическими свойствами, таких как имбирь, йогурт, душица, грейпфрут, куркума и чеснок.
6. Риск развития рака.
Чрезмерное использование антибиотиков может вызвать окислительный стресс и увеличивает риск развития некоторых видов рака — толстого кишечника, молочной железы, печени. Помните, что антибиотиками не лечат вирусные инфекции (грипп, ОРВИ, гepпeс) и не принимайте их без острой необходимости.
7. Повреждение функции почек.
Некоторые антибактериальные препараты, такие как метициллин, ванкомицин, сульфаниламиды, гентамицин, фторхинолоны, гатифлоксацин, левофлоксацин, моксифлоксацин, стрептомицин могут быть вредны для ваших почек. Исследования обнаружили увеличение риска острого повреждения почек у мужчин, принимающих фторхинолоны.
Почки удаляют ненужные вещества, регулируют баланс воды и минералов в крови, даже небольшое повреждение них может вызвать серьезные проблемы. Если у вас есть почечная патология, сообщите о ней врачу для корректирования приёма лекарств. А если при приёме антибиотиков вы заметили изменения в мочеиспускании, отёки, тошноту и рвоту, обратитесь к врачу.
Читать еще: Лечение аллергии на комариные укусы у взрослого и ребенка
8. Инфекции мочевыводящих путей.
Антибиотики, используемые для лечения некоторых заболеваний, могут вызывать инфекции мочевыводящих путей (ИМП), особенно у детей. Они часто уничтожают полезные бактерии, живущие вблизи мочеиспускательного канала и способствуют росту опасных микроорганизмов в мочевых путях и мочевом пузыре. ИМП можно предотвратить, практикуя правила личной гигиены.
9. Заболевания внутреннего уха.
Все члeны семейства антибиотиков-аминогликозидов токсичны для внутреннего уха, куда препарат может попасть через кровеносную систему или путем диффузии из среднего уха во внутреннее. Более высок риск ототоксичности при использовании аминогликозидов у тех, кто принимает наркотики. Симптомы ототоксичности — частичная или глубокая потеря слуха, головокружение и шум в ушах (временные или постоянные).
10. Снижение эффективности пpoтивoзaчaточных таблеток.
Если вы принимаете таблетки для предупреждения беременности, рифампицин и подобные препараты могут снизить их эффективность. Это подтверждено исследованиями. При приёме антибиотиков, если вам необходимо использовать кoнтpaцепцию, попросите гинеколога предложить другие методы кoнтpaцепции, такие как инъекции прогестагена, внутриматочные устройства.
Как принимать антибиотики без вреда для здоровья.
- Помните, что побочные эффекты отличаются у разных людей и от разных антибиотиков.
- Во время приёма антибактериальных препаратов пейте много воды, чтобы избежать обезвоживания.
- Избегайте алкоголя и кофеина.
- Избегайте употрeбления острой пищи, переключитесь на мягкие диеты.
- Не принимайте лекарства без рецепта врача.
- Пройдите весь курс лечения, чтобы организм получил нужную дозировку.
- Никогда не принимайте оставшиеся после курса лечения препараты.
- Не принимайте антибиотики, выписанные для кого-то ещё. Ваши инфекционные бактерии могут отличаться от тех, для которых лекарство было рекомендовано.
- Не давите на врача, чтобы он назначил вам антибиотики для скорейшего выздоровления. Вместо этого спросите о методах облегчения симптомов.
- Используйте природные продукты-антибиотики, такие как имбирь, йогурт, мёд, душица, грейпфрут, куркума, чеснок для борьбы с инфекциями.
Если статья показалась вам полезной, поделитесь с друзьями в социальных сетях.
Как действуют антибиотики на организм, их плюсы и минусы
Антибиотики – это препараты, которые уничтожают патогенную микрофлору или сдерживают интенсивность ее размножения. Однако препараты не всегда обладают избирательным действием. Часто антибактериальные средства нeблагоприятно влияют на естественную флору, которая обитает в кишечнике человека и выполняет ряд важных функций. Без симбионтных бактерий невозможно нормальное пищеварение. Поэтому необходимо знать, как работают антибиотики и как их правильно принимать.
Механизм действия антибиотиков, их преимущества и недостатки
Главным эффектом от применения антибактериальных средств является уничтожение патогенных бактерий. При их проникновении в организм в тканях развивается воспалительная реакция и формируется инфильтрат, в котором размножаются микроорганизмы. Иногда распространение микроорганизмов сдерживается компонентами иммунитета – лимфоцитами, нейтрофилами, макрофагами. Однако при высокой патогенности вредного микроорганизма иммунитет не способен полностью уничтожить инфекцию.
В таком случае и требуется назначение антибактериальных средств. Действующее вещество некоторых препаратов проникает в очаг инфекции и уничтожает микроорганизмы напрямую, приводя к их гибели. Такое действие называется бактерицидным.
Другие лекарственные средства влияют на размножение микроорганизмов. Препараты тормозят активность синтеза белков и нуклеиновых кислот в клетке бактерии, вследствие чего микроорганизм не может размножаться. Численность патогенов резко снижается, оставшиеся бактерии уничтожаются иммунными клетками. Благодаря этому активность инфекции снижается.
- выраженный антибактериальный эффект;
- борьба с воспалительным процессом;
- купирование тяжелых инфекций за несколько дней;
- восстановление нормальной стерильности тканей.
- при перopaльном приеме – уничтожение бактерий нормальной микрофлоры, которое может привести к выраженному дисбактериозу;
- различные побочные эффекты (влияние на кроветворение, пищеварительную систему, метаболизм печени и т.д.);
- возможность передозировки при неаккуратном лечении.
Можно ли самостоятельно назначать себе антибиотики?
Самостоятельно покупать и использовать антибиотики строго запрещено, поэтому препараты отпускаются только по рецепту врача. Такое решение связано с выраженными побочными эффектами препарата. Пациенты должны понимать, что они не могут самостоятельно продумать все тонкости назначения:
- Оценить необходимость применения препарата. Многие люди хотят использовать антибактериальные средства при простейших инфекциях, хотя без них можно и обойтись. Лекарства данной группы не являются универсальными, антибиотики назначают только тогда, когда обойтись без них нельзя.
- Установить природу заболевания. Инфекция может быть не только бактериальной, но и вирусной, грибковой, протозойной. Против этих возбудителей антибиотики совершенно неэффективны. Отличить простуду от гриппа или ОРВИ без медицинской подготовки, конечно, можно, однако в большинстве случаев анализ клинической картины заболевания лучше проводить врачу.
- Подобрать подходящий препарат. Существует множество групп антибиотиков, каждая из которых имеет тропность к определенным микроорганизмам.
- Оценить риски использования средства. Пациент не способен самостоятельно проанализировать свое состояние и подобрать подходящее лекарство. Особенно это касается людей, у которых имеются какие-либо хронические заболевания. Они могут быть противопоказаниями к использованию того или иного препарата, вследствие чего бесконтрольное употрeбление этого лекарства нанесет вред пациенту и усугубит течение его болезни.
- Подобрать дозировку. Антибиотики – это препараты, которые должны принимать строго в определенные временные промежутки. Это необходимо для того, чтобы в организме пациента постоянно поддерживалась высокая концентрация действующего вещества, сдерживающего размножение бактерий. Точно установить порядок использования лекарства может только врач.
Когда прием антибиотиков оправдан?
Антибиотики применяются при местных и генерализованных инфекциях:
- бронхит, пневмония;
- менингит, энцефалит;
- аппендицит, холецистит, панкреатит;
- колит, колиэнтерит;
- фарингит, ларингит в тяжелых формах;
- гeнитaльные инфекции, передающиеся пoлoвым путем (сифилис, гoнopeя);
- цистит, уретрит, пиелонефрит;
- раневые инфекции;
- образование абсцессов, фурункулов, карбункулов.
Есть ли альтернатива антибиотикам?
Антибиотики – это уникальная группа препаратов, полной альтернативы которым практически нет. Применение народных средств, местных антисептиков эффективно при инфекциях с низкой степенью активности. При выраженных местных процессах лучше применять антибактериальные препараты.
Косвенное антибактериальное воздействие могут оказывать препараты из группы иммуностимуляторов. Это лекарства ускоряют выработку иммунных клеток, благоприятно влияют на состояние гумopaльной системы. Активированный иммунитет более эффективно борется с инфекцией в организме.
На данный момент разpaбатываются новые препараты, которые могут заменить антибиотики. Это лекарства, содержащие элементы бактериофагов – вирусов патогенных бактерий. Агенты внедряются в болезнетворные микроорганизмы и уничтожают их изнутри. При этом фаги не оказывают системного эффекта, которое является главным недостатком антибиотиков.
Какие бывают бактериофаги:
- сальмонеллёзный;
- протейный;
- коли;
- колипротейный;
- стрептококковый;
- стафилококковый;
- дизентерийный;
- синегнойной палочки;
- клебсиелл и т. д.
Выпускаются они виде растворов для наружного и внутреннего применения, некоторые существуют и в виде таблетированной формы.
Антибиотики. Их влияние на организм и микрофлору
Речь пойдет о антибиотиках, эдакой «тяжелой артиллерии» современной медицины. Все знают, что это эффективное средство против инфекционных болезней… при куче противопоказаний. Тем не менее широко применяемое. Человек, познакомившийся с медициной вплотную, обязательно столкнулся с этими препаратами и прочувствовал на своей шкуре всю «подлость» их применения. Соскочить с конвейера сопутствующих такому лечению проблем достаточно трудно, и дальнейшее восстановление здоровья в такой ситуации потребует значительных усилий.
Это статья о понимании принципов работы антибиотиков, о их негативном влиянии на наш организм и микрофлору.
Антибиотики — история создания
Если в пару словах, то антибиотики — это вещества, способные подавлять рост микроорганизмов или полностью их уничтожить.
Прародитель современных антибиотиков, пенициллин, был открыт Александром Флемингом еще в 1928г. Первые его версии работали очень не стабильно, и напоминали современные лекарства от рака: никто не мог дать гарантию, кто быстрее погибнет, пациент или бактерии, возбудители болезни. Чуть позже были выделены чистые формы антибиотика, что конечно смягчило ситуацию. Это было революционное открытие в медицине и очень своевременное: пенициллин во времена 2-й мировой спас просто огромное число жизней, и сколотил состояния тем, кто его изготовлял. Учитывая времена и нехватку лекарств, его применение было оправдано. С этого, пожалуй, и началась вера болеющих в «панацею» антибиотиков, и взятие их на вооружение медицины, как основы борьбы с вирусами , с бактериальными недугами и грибковыми инфекциями
Это было в прошлом. А в будущем нам только и осталось, что разгрeбaть последствия этого изобретения и его бездумных применений. И с каждым новым поколением работы прибавляется. И это самое «подлое»: негативные эффекты накапливаются и значительно проявляются в основном спустя поколения. Вспомните здоровье наших отцов, дедов — они, питаясь не самым лучшим образом, тем не менее, имели в большинстве достаточно крепкое здоровье. Теперь же болезни обрушиваются буквально с пеленок. Причем те из них, которые были присущи только взрослым. Да, проблема тут не только в антибиотиках, но именно их применение закладывает фундамент, притягивающий огромное количество проблем.
Читать еще: Повышают защитные свойства организма
Негативные воздействия и влияние антибиотиков на наш организм
Даже самое извpaщeнное питание не способно так «ломать» нас и наш микромир, как «лечение» антибиотиками. Последняя сотня лет со времен открытия пенициллина и последующего нарастающего применения его вариаций по поводу и без, дала больше проблем со здоровьем, чем все предыдущие человеческие «шалости» на протяжении веков.
Вот некоторые последствия применения антибиотиков:
- Подавление, как симбиотической микрофлоры, так и «враждебной». Создает территорию «отсутствия жизни» внутри нас, в которой в состоянии поселиться только бактерии с выработанной устойчивостью.
- Нарушение механизмов нашей системы «энергодобычи». Нарушается клеточное дыхание, что постепенно переводит организм в анаэробное состояние, ограничивая доступ кислорода к тканям.
- Антибиотики годаздо сильнее алкоголя и жиров «садят» печень, забивая её желчные проходы. Печень практически лишается способности накапливать гликоген. Как следствие обилие проблем: вялость, слабость, неуемный аппетит, гиподинамия. В уже поврежденную печень практически гарантированно заселяются паразиты.
- Быстро истощают буферные системы печени, призванные компенсировать токсические воздействия. Как следствие их недостатка — повышенный вред от ядов, болезни. Печень меняет свои функции: вместо очищения начинает загрязнять нас.
- Буквально «выключают» наш иммунитет.
Это часть пагубного воздействия, свойственная большинству видов антибиотиков. Остальные вариации вредностей будут зависеть от конкретных их видов. Благо их сегодня неисчислимые количества.
Антибиотики и микрофлора
Основное влияние антибиотиков, как известно, направлено на сдерживание роста микрофлоры и её уничтожение.
Многие виды препаратов изготовляют из грибов, ввиду их свойств подавлять окружающий микромир. Микробы-грибки активны и «враждебны» к большинству бактерий и достаточно устойчивы к их влиянию. Такие грибки — настоящие «варвары»микромира. Хотя есть и другие виды, которые используются в изготовлении препаратов, «подстегующих» наш иммунитет.
Организм и вся его населяющая микрофлора образуют устойчивый гомеостаз. Именно устойчивость и баланс всех процессов и взаимодействие с населяющими нас микробами определяет качество нашей жизнедеятельности. Любой антибиотик — ингибитор. Он подавляет жизненно важные химические реакции микробов, что приводит к их гибели. Применение любого такого препарата — серьезный «перекос» нашего гомеостаза и устойчивости микромира.
Антибиотики обеспечивают непродолжительную «стерильность» внутри нас. Что многими ошибочно трактуется как «благо», ввиду непонимания роли микрофлоры в нашей жизни. Именно её развитие у человека является наивысшим «приобретением» в эволюции, и именно благодаря сожительству с симбиотическими микроорганизмами мы обретаем наивысшую приспосабливаемость, иммунитет и гибкость среди всех живых существ. Любой серьезный перекос, который организму не удалось компенсировать, запускает по принципу домино череду серьезных нарушений и патологий!
Длительное применение антибиотиков создает среду в организме, в которой никто кроме самих молекул грибов и паразитов уже не может существовать. Расхожее мнение о том, что микрофлора быстро восстановится после такой бомбежки, — ошибочно. Она не вырастет, среда не позволит, а только дополнится пришедшими. А кто придет, пока иммунитет отключен? Те, кто будет обладать резистивностью к воздействию препарата, и на фоне «пробитого» иммунитета и задавленности микроорганизмов-конкурентов обязательно вспыхнут новыми проблемами. Болезнями.
Широко известен факт, что антибиотики своим воздействием расшатывают т.н. «грибо-бактериальное равновесие» в организме. Когда бактерии беспощадно «убивались» грибками и последние начинали преобладать, медики додумались дополнительно вводить противогрибковый препарат «Нистанин», дабы сдержать агрессию. Потом стало заметно, что на фоне всего этого падает иммунитет — и ему догадались помочь таблеткой. И т.д. Убивая одних — размножаются другие. Убиваем других — размножаются вообще кто не попадя. Так мы плавно «на волне» антибиотиков стремимся к стерильности. Которая для нас — cмepть.
Природные антибиотики
Микромир в каждый момент времени «сражается» за территории. В природе есть бактерии симбионты, а есть враги. Большинство искусственных антибиотиков направлены на широкий спектр микробов, и они создают условия нeблагоприятные для наших бактерий-симбионтов. Природные же «лекарства» более щадящие к дружественным нам «сожителям».
Самые известные природные антибиотики это чеснок, лук, острый перец и различные травы. Они отлично подавляют патогенов, хотя и «друзьям» достается. Поэтому в ситуациях когда первые явно преобладают, прием в пищу спец еды конечно оправданы. И первый признак того, что природные антибиотики необходимы — зов организма. Запах будет просто сводить с ума — вы не пропустите тяги на чеснок либо лук.
Естественная «версия» препаратов отличается от созданной в лабораторных условиях количеством побочных воздействий. Они минимальны. Если медицине вторичен вред, нанесенный печени и нашим тканям, то природе нет. Но все же ущерб возможен, хоть и с легкостью компенсируем, поэтому употрeбление этих продуктов в пищу здоровому человеку лишен необходимости.
Еще хочется дополнительно упомянуть о таком «целителе», как кислород. Обильно поступающий в кровь, он убивает анаэробных организмов, которыми и являются многие болезнетворы, являясь своего рода антибиотиком, который лишен изъянов. Обилие кислорода в тканях — норма для человека, и лучшая его «накачка» — аэробные нагрузки. Это «укол» жизненной энергии для нас.
Современно питание, химическое отравление среды и конечно применение антибиотиков привели практически всех людей к анаэробному существованию. Большинство средств современной медицины сводят на нет наш иммунитет и нарушают нормальную жизнедеятельность тканей и органов. Перспективы не радужные. Сегодня даже в большинстве минеральной воды в составе содержатся антибиотики. Это препятствует её порче и продлевает сохранение товарного вида. Антибиотики все больше превращаются в подобие снежного кома, который выгоден производителю, но не потребителю. Микробы к антибиотикам приспосабливаются довольно быстро, что заставляет все более развивать фармацевтику и бесконечно улучшать препараты. Заодно и генерировать новые патологии, которые мы исправно копим и передаем потомству. Если от болезней, вызванных неправильным питанием, излечиться достаточно просто, то после усиленного «лечения» медицины доза приложенных усилий несказанно растет.
Но основная проблема использования препаратов именно в нашей лени. Не лени врачей, ставящих диагноз и приписывающие соответствующее лечение, хотя и их она стороной не обошла, — а прежде всего нашей. Она, в сумме с безответственностью и безграмотностью относительно вопросов здоровья, вынуждает применять антибиотики при малейших послаблениях и простудах. Даже в лечении своих детей. Большинство применяющих даже не знают того, что антибиотики абсолютно бесполезны против вирусных инфекций.
Как думаете сколько человек, при диагнозе и приписке курса антибиотиков «погуглит» в интернете причины тревожащих симптомов, поставленный диагноз, назначенный препарат? Единицы. А те, кто «осмелился» это сделать — быстро нашли альтернативные пути более адекватного и эффективного лечения.
Всего комментариев: 32
Юрий, спасибо за статью, очень познавательно. Нужен Ваш совет. Пила антибиотик 7 дней, после него еще назначены свечи для поднятия иммунитета и свечи для восстановления микрофлоры. Но на 7 день приема антибиотиков, после разговора с братом, решила больше не пить никакие лекарства, а перейти на сыроедение, что в тот же день и сделала. Теперь я на сыроедении всего лишь 4-й день, пока все отлично, удивило то, что хочется есть все по отдельности. Вопрос такой: как Вы считаете, стоит ли мне применять прописанные свечи или этим я только сделаю хуже организму. Вроде решила от них отказаться, а теперь сомневаюсь…Что вы думаете если делать самомассаж в домашних условиях.
Алиса, я думаю только вы знаете как может отреагировать на это действие Ваш организм. А что могу подсказать я? Не зная Вас, вашего организма, даже причин употрeбления антибиотиков? Все слишком индивидуально.
Антибиотики сажают печень и вредят микрофлоре, сейчас только ими и лечат, поэтому приходится принимать доп препараты гепатопротекторы иначе к старости будет совсем худо, когда мне назначали курс урсосана я только расстраивалась — опять пить таблетки, теперь думаю только о том как хорошо что мне его назначали, без него пришлось бы сильно себя ограничивать чтобы не навредить печени, а так даже обследования показывают что сейчас она в очень хорошем состоянии.
Интересная статья,очень полезно знаь такие вещи!
Важно знать родителям о здоровье:
FitoSpray для похудения (Фитоспрей)
FitoSpray для похудения ( Фитоспрей) FitoSpray — спрей для похудения Многие мечтают похудеть, стать стройными, обрести фигуру мечты. Неправильное питание,…
07 03 2023 13:55:55
Фитостеролы в продуктах питания
Фитостеролы в продуктах питания Фитостерины Существует много питательных веществ, которые, как утверждают исследователи, могут положительно повлиять на…
06 03 2023 14:22:48
Фитотерапевт
Фитотерапевт Фитотерапевт Я, Ирина Гудаева — травница, массажист, ведущая семинаров по созданию натуральной косметики и курса « Практическое травоведение»…
05 03 2023 3:12:23
Fitvid
Fitvid Брекеты: минусы, трудности, проблемы Брекет-системы помогли избавиться от комплексов миллионам людей. Это действительно эффективный инструмент,…
04 03 2023 0:40:44
Фониатр
Фониатр Фониатрия – один из разделов медицины. Фониатры изучают патологии голоса, методы их лечения, профилактики, а также способы коррекции…
01 03 2023 10:15:19
Форель
Форель Форель относится к отряду лососеобразных, семейству лососевых. Ее тело удлинено, немного сжато с боков, покрыто мелкой чешуей. Замечательной…
28 02 2023 18:48:59
Формула идеального веса
Формула идеального веса Калькулятор нормы веса Вес 65 кг относится к категории Норма для взрослого человека с ростом 170 см . Эта оценка основана на…
25 02 2023 23:15:27
Формулы расчета идеального веса
Формулы расчета идеального веса Фoрмулa «идeальнoго вeса» То, что ожирение шагает семимильными шагами по планете – это факт. И, несмотря на то, что…
24 02 2023 18:31:10
Фосфатида аммонийные соли
Фосфатида аммонийные соли Аммонийные соли фосфатидиловой кислоты ( Е442) Е442 – это пищевая добавка, которую относят к категории эмульгаторов. Вещество…
23 02 2023 7:41:15
Фототерапия новорожденных
Фототерапия новорожденных Фототерапия новорожденных Применение фототерапии для новорожденных С момента своего рождения организм ребенка начинает адаптацию…
22 02 2023 21:23:16
Фототерапия новорожденных при желтухе
Фототерапия новорожденных при желтухе Фототерапия новорожденных После появления ребенка на свет его организм адаптируется к совершенно иным условиям…
21 02 2023 18:18:14
Французская диета
Французская диета Французская диета Эффективность: до 8 кг за 14 дней Сроки: 2 недели Стоимость продуктов: 4000 рублей на 14 дней Общие правила…
20 02 2023 5:41:10
Фрукт Кумкват — что это такое?
Фрукт Кумкват — что это такое? Фрукт Кумкват — что это такое? Впервые упоминают необычный для европейцев фрукт китайские летописи 11 века. Португальские…
19 02 2023 9:15:19
Фруктовая диета
Фруктовая диета Фруктовая диета Эффективность: 2-5 кг за 7 дней Сроки: 3-7 дней Стоимость продуктов: 840-1080 рублей в неделю Общие правила Фруктовая…
17 02 2023 20:55:27
Фруктоза при диабете
Фруктоза при диабете Можно ли фруктозу при сахарном диабете? Для многих диабет является той проблемой, которая вносит в жизнь ряд ограничений. Так, к…
14 02 2023 8:36:41
Фрукт свити – польза и вред
Фрукт свити – польза и вред Свити — что это за фрукт? Что такое свити? Продолжаем разбирать цитрусовые, но как всегда идем не по верхам, а копаем глубже и…
11 02 2023 5:53:25
Фрукты и ягоды
Фрукты и ягоды Разница между фруктом и ягодой Фрукты и ягоды любят практически все. Ведь они такие вкусные и полезные! Мы любуемся лежащими на столе…
10 02 2023 14:36:11
Фтизиатр
Фтизиатр Врачи фтизиатры Москвы Фтизиатр — это дипломированный специалист в области фтизиатрии. Он специализируется на профилактике, диагностике, лечении…
08 02 2023 9:43:35
Фтор в организме человека
Фтор в организме человека Фтор в организме человека Дневная норма потрeбления Мужчины старше 60 лет Женщины старше 60 лет Беременные (2-я половина)…
07 02 2023 13:12:58
Боли в спине после рождения ребёнка
Боли в спине после рождения ребёнка Почему после родов болит спина У мамочек нередко болит спина после родов. Причем, дискомфорт может длиться довольно…
04 02 2023 2:33:38
Фунчоза: польза и вред
Фунчоза: польза и вред Фунчоза: польза и возможный вред Увлечение восточной кухней год от года растет. Принято считать, что такой рацион полезен для…
03 02 2023 18:15:15
Фундук
Фундук В рационе здорового человека обязательно присутствуют орехи в различных вариациях. Среди них выгодно выделяется фундук. Высокая пищевая ценность и…
02 02 2023 20:45:26
Галактоза
Галактоза Галактоза – это представитель класса простых молочных сахаров. В человеческий организм поступает преимущественно в составе молока,…
29 01 2023 4:18:26
Галанга
Галанга С древних времен растения играют важную роль в жизни человека, в том числе и для поддержания здоровья. Некоторые травы известны как лучшие…
28 01 2023 13:45:49
Галега лекарственная
Галега лекарственная Галега лекарственная (Galega officinalis) Син: козлятник лекарственный, козлятник аптечный, козья рута, французская сирень, солодянка…
27 01 2023 3:27:57
Боли в суставах при беременности
Боли в суставах при беременности Боли в суставах при беременности В период беременности у женщины могут возникать различные боли в самых разных местах….
24 01 2023 15:43:51
Гастрит и изжога
Гастрит и изжога Лучшие лекарства от изжоги и гастрита Многие пациенты с гастритом и другими заболеваниями Ж К Т страдают от изжоги. Данный симптом может…
23 01 2023 18:35:34
Где находится ключица у человека на фото?
Где находится ключица у человека на фото? Ключица человека: анатомия, строение, функции Ключица – это единственное костное образование в теле человека,…
20 01 2023 11:10:31