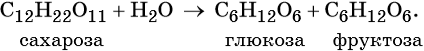Биологически важные вещества: жиры, белки, углеводы (моносахариды, дисахариды, полисахариды). Теория для ЕГЭ по химии.
Жиры: получение и свойства
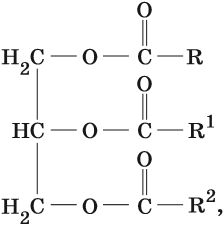
Жиры – это сложные эфиры, образованные глицерином и высшими одноосновными карбоновыми кислотами (жирными кислотами).
.
Жиры образуются при взаимодействии глицерина и высших карбоновых кислот:
| Жирные (высшие) кислоты | |
| Предельные кислоты | Непредельные кислоты |
| Масляная кислота С3Н7 -СООН | Олеиновая кислота С17Н33СООН
(содержит одну двойную связь в радикале) СН3—(СН2)7—СН = СН—(СН2)7—СООН |
| Пальмитиновая кислота С15Н31 — СООН | Линолевая кислота С17Н31СООН
(две двойные связи в радикале) СН3-(СН2)4-СН = СН-СН2-СН = СН-СООН |
| Стеариновая кислота С17Н35 — СООН | Линоленовая кислота С17Н29СООН
(три двойные связи в радикале) СН3СН2СН=CHCH2CH=CHCH2CH=СН(СН2)4СООН |
Номенклатура жиров
Общее название жиров – триацилглицерины (триглицериды).
Существует несколько способов назвать молекулу жира.
Например, жир, образованный тремя остатками стеариновой кислоты, будет иметь следующие названия:
Физические свойства жиров
Жиры растворимы в органических растворителях и нерастворимы в воде. С водой жиры не смешиваются.
| Животные жиры — предельные | Растительные жиры (масла) — непредельные |
| Твёрдые, образованы предельными кислотами – стеариновой и пальмитиновой.
Все животные жиры, кроме рыбьего – твёрдые. |
Жидкие, образованы непредельными кислотами – олеиновой, линолевой и другими.
Все растительные жиры, кроме пальмового масла – жидкие. |
Химические свойства жиров
1. Гидролиз (омыление) жиров
Жиры подвергаются гидролизу в кислой или щелочной среде или под действием ферментов.
1.1. Кислотный гидролиз
Под действием кислот жиры гидролизуются до глицерина и карбоновых кислот, которых входили в молекулу жира.
Например, при гидролизе тристеарата глицерина в кислой среде образуется стеариновая кислота и глицерин
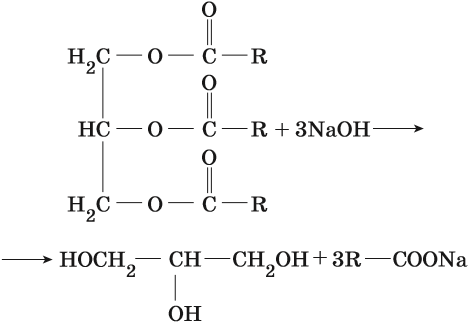
1.2. Щелочной гидролиз — омыление жиров
При щелочном гидролизе жиров образуется глицерин и соли карбоновых кислот, входивших в состав жира.
Например, при гидролизе тристеарата глицерина гидроксидом натрия образуется стеарат натрия.
2. Гидрирование (гидрогенизация) ненасыщенных жиров
Гидрогенизация жиров — это процесс присоединения водорода к остаткам непредельных кислот, входящих в состав жира.
При этом остатки непредельных кислот переходят в остатки предельных, жидкие растительные жиры превращаются в твёрдые (маргарин).
Например, триолеат глицерина при гидрировании превращается в тристеарат глицерина:
Количественной характеристикой степени ненасыщенности жиров служит йодное число, показывающее, какая масса йода может присоединиться по двойным связям к 100 г жира.
3. Мыло и синтетические моющие средства
При щелочном гидролизе жиров образуются мыла – соли высших жирных кислот.
Стеарат натрия – твёрдое мыло.
Стеарат калия – жидкое мыло.
Моющая способность мыла зависит от жесткости воды. Оно хорошо мылится и стирает в мягкой воде, плохо стирает в жёсткой воде и совсем не стирает в морской воде, так как содержащие в ней ионы Ca2+ и Mg2+ дают с высшими кислотами нерастворимые в воде соли.
Например, тристеарат глицерина взаимодействует с сульфатом кальция
Поэтому наряду с мылом используют синтетические моющие средства.
Их производят из других веществ, например из алкилсульфатов — солей сложных эфиров высших спиртов и серной кислоты.
Спирт реагирует с серной кислотой с образованием алкилсульфата.
Далее алкилсульфат гидролизуется щелочью:
Эти соли содержат в молекуле от 12 до 14 углеродных атомов и обладают очень хорошими моющими свойствами. Кальциевые и магниевые соли этих веществ растворимы в воде, а потому такие мыла моют и в жесткой воде. Алкилсульфаты содержатся во многих стиральных порошках.
Белки
Белки (полипептиды) – биополимеры, построенные из остатков α-аминокислот, соединенных пептидными (амидными) связями.
Образование белковой макромолекулы можно представить как реакцию поликонденсации α-аминокислот:
Макромолекулы белков имеют стереорегулярное строение, исключительно важное для проявления ими определенных биологических свойств.
Структуры белков
Химические свойства белков
Качественные реакции на белки
- Биуретовая реакция – фиолетовое окрашивание при действии на белки свежеосажденного гидроксида меди (II).
Видеоопыт взаимодействия белка с гидроксидом меди (II) можно посмотреть здесь.
- Ксантопротеиновая реакция – желтое окрашивание при действии на белки концентрированной азотной кислоты.
Видеоопыт взаимодействия белка с концентрированной азотной кислотой можно посмотреть здесь.
Денатурация белка
Это разрушение структуры белка при нагревании, изменении кислотности среды, действии излучения, спирта, тяжелых металлов, радиации.
Пример денатурации — свертывание яичных белков при варке яиц.
Видеоопыт денатурации белка можно посмотреть здесь.
Денатурация бывает обратимой и необратимой.
- При обратимой денатурации первичная структура белка не разрушается.
- Необратимая денатурация может быть вызвана образованием нерастворимых веществ при действии на белки солей тяжелых металлов — свинца или ртути.
- При необратимой денатурации происходит также гидролиз белка — необратимое разрушение первичной структуры в кислом или щелочном растворе с образованием аминокислот или более коротких пептидных фрагментов.
Анализируя продукты гидролиза, можно установить количественный состав белков.
Углеводы
Углеводы (сахара) – органические соединения, имеющие сходное строение, состав большинства которых отражает формула Cx(H2O)y, где x, y ≥ 3.
Исключение составляет дезоксирибоза, которая имеют формулу С5Н10O4 (на один атом кислорода меньше, чем рибоза).
Классификация углеводов
По числу структурных звеньев
- Моносахариды — содержат одно структурное звено.
- Олигосахариды — содержат от 2 до 10 структурных звеньев (дисахариды, трисахариды и др.).
- Полисахариды — содержат n структурных звеньев.
Некоторые важнейшие углеводы:
| Моносахариды | Дисахариды | Полисахариды |
| Глюкоза С6Н12О6
Фруктоза С6Н12О6 Рибоза С5Н10О5 Дезоксирибоза С5Н10О4 |
Сахароза С12Н22О11
Лактоза С12Н22О11 Мальтоза С12Н22О11 Целлобиоза С12Н22О11 |
Целлюлоза (С6Н10О5)n
Крахмал(С6Н10О5)n |
По числу атомов углерода в молекуле
- Пентозы — содержат 5 атомов углерода.
- Гексозы — содержат 6 атомов углерода.
- И т.д.
По размеру кольца в циклической форме молекулы
- Пиранозы — образуют шестичленное кольцо.
- Фуранозы — содержат пятичленное кольцо.
Химические свойства, общие для всех углеводов
1. Горение
Все углеводы горят до углекислого газа и воды.
Например, при горении глюкозы образуются вода и углекислый газ
C6H12O6 + 6O2 → 6CO2 + 6H2O
2. Взаимодействие с концентрированной серной кислотой
Концентрированная серная кислота отнимает воду от углеводов, при этом образуется углерод С («обугливание») и вода.
Например, при действии концентрированной серной кислоты на глюкозу образуются углерод и вода
C6H12O6 → 6C + 6H2O
Моносахариды
Моносахариды – гетерофункциональные соединения, в состав их молекул входит одна карбонильная группа (группа альдегида или кетона) и несколько гидроксильных.
Моносахариды являются структурными звеньями олигосахаридов и полисахаридов.
Важнейшие моносахариды
| Название и формула | Глюкоза
C6H12O6 |
Фруктоза
C6H12O6 |
Рибоза
C5H10O5 |
| Структурная формула |  |
 |
 |
| Классификация |
|
|
|
Глюкоза
Глюкоза – это альдегидоспирт (альдоза).
Она содержит шесть атомов углерода, одну альдегидную и пять гидроксогрупп.
Глюкоза существует в растворах не только в виде линейной, но и циклических формах (альфа и бета), которые являются пиранозными (содержат шесть звеньев):
Химические свойства глюкозы
Водный раствор глюкозы
В водном растворе глюкозы существует динамическое равновесие между двумя циклическими формами — α и β и линейной формой:
Качественная реакция на многоатомные спирты: реакция со свежеосажденным гидроксидом меди (II)
При взаимодействии свежеосажденного гидроксида меди (II) с глюкозой (и другими моносахаридами происходит растворение гидроксида с образованием комплекса синего цвета.
Реакции на карбонильную группу — CH=O
Глюкоза проявляет свойства, характерные для альдегидов.
- Реакция «серебряного зеркала»
- Реакция с гидроксидом меди (II) при нагревании. При взаимодействии глюкозы с гидроксидом меди (II) выпадает красно-кирпичный осадок оксида меди (I):
- Окисление бромной водой. При окислении глюкозы бромной водой образуется глюконовая кислота:
- Также глюкозу можно окислить хлором, бертолетовой солью, азотной кислотой.
Концентрированная азотная кислота окисляет не только альдегидную группу, но и гидроксогруппу на другом конце углеродной цепи.
- Каталитическое гидрирование. При взаимодействии глюкозы с водородом происходит восстановление карбонильной группы до спиртового гидроксила, образуется шестиатомный спирт – сорбит:
- Брожение глюкозы. Брожение — это биохимический процесс, основанный на окислительно-восстановительных превращениях органических соединений в анаэробных условиях.
Спиртовое брожение. При спиртовом брожении глюкозы образуются спирт и углекислый газ:
C6H12O6 → 2C2H5OH + 2CO2
Молочнокислое брожение. При молочнокислом брожении глюкозы образуется молочная кислота:
Маслянокислое брожение. При маслянокислом брожении глюкозы образуется масляная кислота (внезапно):
- Образование эфиров глюкозы (характерно для циклической формы глюкозы).
Глюкоза способна образовывать простые и сложные эфиры.
Наиболее легко происходит замещение полуацетального (гликозидного) гидроксила.
Например, α-D-глюкоза взаимодействует с метанолом.
При этом образуется монометиловый эфир глюкозы (α-O-метил-D-глюкозид):
Простые эфиры глюкозы получили название гликозидов.
В более жестких условиях (например, с CH3-I) возможно алкилирование и по другим оставшимся гидроксильным группам.
Моносахариды способны образовывать сложные эфиры как с минеральными, так и с карбоновыми кислотами.
Например, β-D-глюкоза реагирует с уксусным ангидридом в соотношении 1:5 с образованием пентаацетата глюкозы (β-пентаацетил-D-глюкозы):
Получение глюкозы
Гидролиз крахмала
В присутствии кислот крахмал гидролизуется:
(C6H10O5)n + nH2O → nC6H12O6
Синтез из формальдегида
Реакция была впервые изучена А.М. Бутлеровым. Синтез проходит в присутствии гидроксида кальция:
6CH2=On → C6H12O6
Фотосинтез
В растениях углеводы образуются в результате реакции фотосинтеза из CO2 и Н2О:
6CO2 + 6H2O → C6H12O6 + 6O2
Фруктоза
Фруктоза — структурный изомер глюкозы. Это кетоноспирт (кетоза): она тоже может существовать в циклических формах (фуранозы).
Она содержит шесть атомов углерода, одну кетоновую группу и пять гидроксогрупп.
Фруктоза – кристаллическое вещество, хорошо растворимое в воде, более сладкое, чем глюкоза.
В свободном виде содержится в мёде и фруктах.
Химические свойства фруктозы связаны с наличием кетонной и пяти гидроксильных групп.
При гидрировании фруктозы также получается сорбит.
Дисахариды
Дисахариды – это углеводы, молекулы которых состоят из двух остатков моносахаридов, соединенных друг с другом за счет взаимодействия гидроксильных групп (двух полуацетальных или одной полуацетальной и одной спиртовой).
Сахароза (свекловичный или тростниковый сахар) С12Н22О11
Молекула сахарозы состоит из остатков α-глюкозы и β-фруктозы, соединенных друг с другом:
В молекуле сахарозы гликозидный атом углерода глюкозы связан из-за образования кислородного мостика с фруктозой, поэтому сахароза не образует открытую (альдегидную) форму.
Такие дисахариды называют невосстанавливающими, т.е. не способными окисляться.
Сахароза подвергается гидролизу подкисленной водой. При этом образуются глюкоза и фруктоза:
C12H22O11 + H2O → C6H12O6 + C6H12O6
глюкоза фруктоза
Мальтоза С12Н22О11
Это дисахарид, состоящий из двух остатков α-глюкозы, она является промежуточным веществом при гидролизе крахмала.
Мальтоза является восстанавливающим дисахаридом (одно из циклических звеньев может раскрываться в альдегидную группу) и вступает в реакции, характерные для альдегидов.
При гидролизе мальтозы образуется глюкоза.
C12H22O11 + H2O → 2C6H12O6
Полисахариды
Полисахариды — это природные высокомолекулярные углеводы, макромолекулы которых состоят из остатков моносахаридов.
Основные представители — крахмал и целлюлоза — построены из остатков одного моносахарида — глюкозы.
Крахмал и целлюлоза имеют одинаковую молекулярную формулу: (C6H10O5)n, но совершенно различные свойства.
Это объясняется особенностями их пространственного строения.
Крахмал состоит из остатков α-глюкозы, а целлюлоза – из β-глюкозы, которые являются пространственными изомерами и отличаются лишь положением одной гидроксильной группы:
Крахмал
Крахмалом называется полисахарид, построенный из остатков циклической α-глюкозы.
В его состав входят:
- амилоза (внутренняя часть крахмального зерна) – 10-20%
- амилопектин (оболочка крахмального зерна) – 80-90%
Цепь амилозы включает 200 — 1000 остатков α-глюкозы (средняя молекулярная масса 160 000) и имеет неразветвленное строение.
Амилопектин имеет разветвленное строение и гораздо большую молекулярную массу, чем амилоза.
Свойства крахмала
- Гидролиз крахмала: при кипячении в кислой среде крахмал последовательно гидролизуется:
Запись полного гидролиза крахмала без промежуточных этапов:
- Крахмал не дает реакцию “серебряного зеркала” и не восстанавливает гидроксид меди (II).
- Качественная реакция на крахмал: синее окрашивание с раствором йода.
Целлюлоза
Целлюлоза (клетчатка) – наиболее распространенный растительный полисахарид. Цепи целлюлозы построены из остатков β-глюкозы и имеют линейное строение.
Свойства целлюлозы
- Образование сложных эфиров с азотной и уксусной кислотами.
Нитрование целлюлозы.
Так как в звене целлюлозы содержится 3 гидроксильные группы, то при нитровании целлюлозы избытком азотной кислоты возможно образование тринитрата целлюлозы, взрывчатого вещества пироксилина:
Ацилирование целлюлозы.
При действии на целлюлозу уксусного ангидрида (упрощённо-уксусной кислоты) происходит реакция этерификации, при этом возможно участие в реакции 1, 2 и 3 групп ОН.
Получается ацетат целлюлозы – ацетатное волокно.
- Гидролиз целлюлозы.
Целлюлоза, подобно крахмалу, в кислой среде может гидролизоваться, в результате тоже получается глюкоза. Но процесс идёт гораздо труднее.
Всего: 78 1–20 | 21–40 | 41–60 | 61–78
Добавить в вариант
Задания Д14 № 591
Глицерин можно получить в результате гидролиза
1) белка
2) жира
3) крахмала
4) целлюлозы
В состав рыбьего жира входят остатки линоленовой (), олеиновой и предельных карбоновых кислот. Из предложенного перечня выберите два вещества, с которыми может реагировать рыбий жир.
1) аммиачный раствор оксида серебра
2) щелочь
3) водород
4) этанол
5) гидроксид меди (II)
Запишите в поле ответа номера выбранных веществ.
Источник: РЕШУ ЕГЭ
Из предложенного перечня выберите два углевода, которые реагируют с аммиачным раствором оксида серебра.
1) целлюлоза
2) мальтоза
3) рибоза
4) фруктоза
5) сахароза
Запишите номера выбранных ответов.
Из предложенного перечня выберите два углевода, которые не реагируют с аммиачным раствором оксида серебра.
1) лактоза
2) рибоза
3) сахароза
4) мальтоза
5) фруктоза
Запишите номера выбранных ответов.
Из предложенного перечня выберите два вещества, с которыми реагируют глюкоза и целлюлоза.
1) кислород
2) водород
3) сульфат меди (II)
4) уксусная кислота
5) гидроксид железа (III)
Запишите в поле ответа номера выбранных веществ.
Источник: РЕШУ ЕГЭ
Из предложенного перечня выберите все вещества, с которыми реагируют все белки.
1) бромная вода
2) концентрированная соляная кислота
3) водород
4) сероводород
5) концентрированная азотная кислота
Запишите в поле ответа номера выбранных веществ.
Источник: РЕШУ ЕГЭ
Из предложенного перечня выберите два вещества, которые образуются при щелочном гидролизе жира, формула которого
1)
2)
3)
4)
5)
Запишите номера выбранных ответов.
Источник: ЕГЭ по химии 2020. Досрочная волна. Вариант 1
Из предложенного перечня выберите два вещества, которые могут образоваться при гидролизе белков.
1) глицин
2) глицерин
3) серилаланин
4) анилин
5) адипиновая кислота
Запишите номера выбранных ответов.
Из предложенного перечня выберите два вещества, которые могут образоваться при гидролизе природных жиров.
1) этиленгликоль
2) бензойная кислота
3) линолевая кислота
4) пропионовая кислота
5) пальмитиновая кислота
Запишите номера выбранных ответов в порядке возрастания.
Из предложенного перечня выберите два вещества, с которыми реагируют и глюкоза, и целлюлоза.
1) водород
2) сульфат меди (II)
3) уксусная кислота
4) гидроксид железа (III)
5) азотная кислота
Запишите в поле ответа номера выбранных веществ.
Источник: РЕШУ ЕГЭ
Из предложенного перечня выберите все вещества, с которыми реагируют все жиры.
1) водородом
2) гидроксидом натрия
3) перманганатом калия
4) гидроксидом калия
5) бромной водой
Запишите в поле ответа номера выбранных веществ.
Источник: РЕШУ ЕГЭ
Из предложенного перечня выберите два вещества, которые могут образоваться при гидролизе природных жиров.
1)
2)
3)
4) цис
5)
Запишите в поле ответа номера выбранных веществ.
Из предложенного перечня выберите все утверждения, характерные для глюкозы, в отличие от сахарозы.
1) горит с образованием СO2
2) вступает в реакцию «серебряного зеркала»
3) не восстанавливает гидроксид меди(II)
4) не вступает в реакцию поликонденсации
5) не подвергается гидролизу
Запишите в поле ответа номера выбранных утверждений.
Источник: РЕШУ ЕГЭ
Из предложенного перечня выберите два вещества, которые могут образоваться при гидролизе природных белков.
1)
2)
3)
4)
5)
Запишите в поле ответа номера выбранных веществ.
Из предложенного перечня выберите два вещества, с которыми способен взаимодействовать триолеат глицерина.
1) водород
2) бензол
3) натрий
4) гидроксид натрия
5) этанол
Запишите в поле ответа номера выбранных веществ.
Источник: РЕШУ ЕГЭ
Из предложенного перечня выберите два вещества, с которыми способен взаимодействовать тристеарат глицерина.
1) кислород
2) водород
3) гидроксид меди (II)
4) перманганат калия
5) гидроксид натрия
Запишите в поле ответа номера выбранных веществ.
Источник: РЕШУ ЕГЭ
Из предложенного перечня углеводов выберите два, которые дают реакцию «серебряного зеркала».
1) рибоза
2) глюкоза
3) сахароза
4) целлюлоза
5) гликоген
Запишите в поле ответа номера выбранных веществ.
Из предложенного перечня углеводов выберите два, которые могут вступать в реакцию гидролиза.
1) глюкоза
2) фруктоза
3) сахароза
4) рибоза
5) целлюлоза
Запишите в поле ответа номера выбранных веществ.
Из предложенного перечня углеводов выберите два, которые могут вступать в реакцию гидролиза.
1) фруктоза
2) сахароза
3) рибоза
4) дезоксирибоза
5) мальтоза
Запишите в поле ответа номера выбранных веществ в порядке возрастания.
Из предложенного перечня углеводов выберите два, которые дают реакцию «серебряного зеркала».
1) рибоза
2) сахароза
3) крахмал
4) гликоген
5) мальтоза
Запишите в поле ответа номера выбранных веществ в порядке возрастания.
Всего: 78 1–20 | 21–40 | 41–60 | 61–78
Белки — это природные высокомолекулярные соединения (биополимеры), структурную основу которых составляют полипептидные цепи, построенные из остатков альфа-аминокислот.
Все белки являются полипептидами, но не всякий полипептид является белком.
Физические свойства белков:
Свойства белков также разнообразны, как и функции, которые они выполняют. Одни белки растворятся в воде, образуя, как правило, коллоидные растворы (например, белок яйца); другие растворяются в разбавленных растворах солей; третьи нерастворимы (например, белки покровных тканей).
Химические свойства белков — гидролиз белков:
Белки + H2O = полипептиды + H2O = олигопептиды + H2O = дипептиды + H2O = альфа-аминокислоты
(условия реакций везде: кислая среда и нагревание)
Жиры — это смесь сложных эфиров глицерина и высших карбоновых кислот (ВКК)ю
Общая формула жиров:
Физические свойства жиров:
Жиры — вязкие жидкости или твердые вещества, легче воды; в воде не растворяются, но растворяются в органических растворителях (бензине, бензоле и т.д.)
Химические свойства жиров:
1. Гидролиз: водный, кислотный, ферментативный, щелочной.
2. Гидрирование.
3. Присоединение галогенов.
Функции жиров в организме:
1. Энергетическая.
2. Структурная.
3. Защитная.
Углеводы — обширный класс природных соединений, которые играют важную роль в жизни человека, животных и растений.
Простые углеводы (моносахариды) — это простейшие углеводы, не гидролизующиеся с образованием более простых углеводов.
Сложные углеводы — это углеводы, молекулы которых состоят из двух или большего числа остатков моносахаридов и разлагаются на эти моносахариды при гидролизе.
Физические свойства:
Моносахариды представляют собой бесцветные кристаллические вещества, сладкие на вкус, хорошо растворимы в воде, нерастворимы в эфире, плохо растворимы в спирте. Сладость моносахаридов различна. Например, фруктоза слаще глюкозы в три раза.
Химические свойства моносахаридов:
1. Свойства по карбонильной группе в открытых формах моносахаридов.
2. Свойства по спиртовым группам как в открытых, так и в циклических формах моносахаридов.
3. Свойства по полуацетальной гидроксильной группе.
- Курс
Меня зовут Быстрицкая Вера Васильевна.
Я репетитор по Химии
Вам нужны консультации по Химии по Skype?
Если да, подайте заявку. Стоимость договорная.
Чтобы закрыть это окно, нажмите «Нет».
Жиры — сложные эфиры глицерина и высших одноосновных карбоновых кислот (так называемых ЖИРНЫХ кислот).
Общее название таких соединений – триглицериды или триацилглицерины, где ацил – остаток карбоновой кислоты
ФИЗИЧЕСКИЕ СВОЙСТВА
Жидкие или твердые вещества, растворимые в органических растворителях, но не растворимые в воде.
ХИМИЧЕСКИЕ СВОЙСТВА.
ГИДРОЛИЗ ЖИРОВ
проходит в кислой или в щелочной среде, или под действием ферментов:
а) кислотный (водный) гидролиз:
под действием кислоты жиры гидролизуются до глицерина и карбоновых кислот, которых входили в молекулу жира.
б) щелочной гидролиз – омыление.
Получают глицерин и соли карбоновых кислот (мыла), входивших в состав жира. Мыла – соли высших жирных кислот (натриевые – твёрдые, калиевые – жидкие).
При пищеварении жир омыляется (расщепляется) с помощью ферментов.
ГИДРИРОВАНИЕ (ГИДРОГЕНИЗАЦИЯ)
процесс присоединения водорода к остаткам непредельных кислот, входящих в состав жира.
Остатки непредельных кислот переходят в остатки предельных, жидкие растительные жиры превращаются в твёрдые (маргарин).
Жидкие жиры обесцвечивают бромную воду, что говорит о наличии двойных связей
УГЛЕВОДЫ (САХАРА) — органические соединения, имеющие сходное строение и свойства, состав большинства которых отражает формула Cx(H2O)y, где x, y ≥ 3.
Исключение составляет дезоксирибоза, которая имеют формулу С5Н10O4.
МОНОСАХАРИДЫ — гетерофункциональные соединения, в состав их молекул входит одна карбонильная группа (альдегидная или кетонная) и несколько гидроксильных.
ФИЗИЧЕСКИЕ СВОЙСТВА МОНОСАХАРИДОВ
Моносахариды – твердые вещества, легко растворимые в воде, плохо – в спирте и совсем нерастворимые в эфире.
Водные растворы имеют нейтральную реакцию на лакмус.
Большинство моносахаридов обладают сладким вкусом, однако меньшим, чем свекловичный сахар.
ХИМИЧЕСКИЕ СВОЙСТВА МОНОСАХАРИДОВ
В водном растворе глюкозы существует динамическое равновесие между двумя циклическими формами — α и β и линейной формой:
СВОЙСТВА ГЛЮКОЗЫ, КАК МНОГОАТОМНОГО СПИРТА
1. Реакция комплексообразование с гидроксидом меди (II).
При взаимодействии свежеосажденного гидроксида меди (II) с моносахаридами происходит растворение гидроксида с образованием комплекса синего цвета.
2. Глюкоза, как альдегид.
Образование сложных эфиров с ангидридами кислот или галогенангидридами.
3. Реакция с гидроксидом меди (II) при нагревании
4. Окисление бромной водой до глюконовой кислоты.
4. Каталитическое гидрирование (восстановление) глюкозы
происходит восстановление карбонильной группы до спиртового гидроксила, получается шестиатомный спирт – сорбит.
5. РЕАКЦИИ БРОЖЕНИЯ.
а) спиртовое брожение
б) молочнокислое брожение
в) маслянокислое брожение
ФРУКТОЗА— структурный изомер глюкозы — КЕТОНОСПИРТ:
Кристаллическое вещество, хорошо растворимое в воде, более сладкое, чем глюкоза. В свободном виде содержится в мёде и фруктах.
Химические свойства фруктозы обусловлены наличием кетонной и пяти гидроксильных групп. При гидрировании фруктозы также получается СОРБИТ.
СВОЙСТВА ДИСАХАРИДОВ
это углеводы, молекулы которых состоят из двух остатков моносахаридов, соединенных друг с другом за счет взаимодействия гидроксильных групп (двух полуацетальных или одной полуацетальной и одной спиртовой).
1. САХАРОЗА (СВЕКЛОВИЧНЫЙ ИЛИ ТРОСТНИКОВЫЙ САХАР) С12Н22О11
Молекула сахарозы состоит из остатков α-глюкозы и β-фруктозы, соединенных друг с другом.
Чистая сахароза — бесцветное кристаллическое вещество сладкого вкуса, хорошо растворимое в воде.
В молекуле сахарозы нет открытой (альдегидной) формы. Вследствие этого сахароза не вступает в реакции альдегидной группы – с аммиачным раствором оксида серебра с гидроксидом меди при нагревании.
Подобные дисахариды называют невосстанавливающими, т.е. не способными окисляться.
2. МАЛЬТОЗА.
Это дисахарид, состоящий из двух остатков α-глюкозы, она является промежуточным веществом при гидролизе крахмала.
Мальтоза — является восстанавливающим дисахаридом и вступает в реакции, характерные для альдегидов.
2. Окисление восстанавливающихся дисахаридов
СВОЙСТВА ПОЛИСАХАРИДОВ.
это природные высокомолекулярные углеводы, макромолекулы которых состоят из остатков моносахаридов.
Основные представители — КРАХМАЛ И ЦЕЛЛЮЛОЗА (C6H10O5)n
Крахмал состоит из остатков α-глюкозы, а целлюлоза – из β-глюкозы, которые являются пространственными изомерами и отличаются лишь положением одной гидроксильной группы (выделена цветом):
КРАХМАЛ.
Крахмалом называется смесь двух полисахаридов, построенных из остатков циклической α-глюкозы. Крахмал — белый порошок, нерастворимый в холодной воде.
В горячей воде он набухает и образует клейстер. В отличие от моно- и олигосахаридов полисахариды не обладают сладким вкусом
2. Гидролиз крахмала
(ферментативный или кислотный) – ведет к образованию глюкозы.
3. Крахмал не дает реакции «серебряного зеркала» и не восстанавливает гидроксид меди (II)
4. Качественная реакция на крахмал — окрашивание поверхности в синий цвет при добавлении раствора йода.
ЦЕЛЛЮЛОЗА
наиболее распространенный растительный полисахаридМолекулярная масса целлюлозы — от 400 000 до 2 млн.
Чистая целлюлоза — твердое белое вещество, имеющее волокнистую структуру. Она нерастворима в воде и органических растворителях, но хорошо растворяется в аммиачном растворе гидроксида меди (II). Как известно, сладкого вкуса целлюлоза не имеет.
Цепи целлюлозы построены из остатков β-глюкозы и имеют линейное строение.
ОБРАЗОВАНИЕ СЛОЖНЫХ ЭФИРОВ.
2. Нитрование целлюлозы
Так как в звене целлюлозы содержится 3 гидроксильные группы, то при нитровании избытком азотной кислоты возможно образование тринитрата целлюлозы, взрывчатого вещества пироксилина:
3. Взаимодействие с уксусной кислотой
Образуется ацетат целлюлозы — ацетатное волокно.
4. Гидролиз целлюлозы (ферментативный или кислотный) — образуется глюкоза
БЕЛКИ (ПОЛИПЕПТИДЫ) — биополимеры, построенные из остатков α-аминокислот, соединенных пептидными (амидными) связями.
Формально образование белковой макромолекулы можно представить как реакцию поликонденсации α-аминокислот
Молекулярные массы различных белков (полипептидов) составляют от 10 000 до нескольких миллионов.Макромолекулы белков имеют стереорегулярное строение, исключительно важное для проявления ими определенных биологических свойств.
Несмотря на многочисленность белков, в их состав входят остатки не более 22 α-аминокислот.
По физическим свойствам белки делят на два класса:
1.ГЛОБУЛЯРНЫЕ БЕЛКИ- растворяются в воде или образуют коллоидныеnрастворы
2.ФИБРИЛЛЯРНЫЕ БЕЛКИ в воде нерастворимы
ДЕНАТУРАЦИЯ БЕЛКА
разрушение вторичной и третичной структуры белка с сохранением первичной структуры. Происходит при нагревании, изменении кислотности среды, действии излучения.
Пример денатурации — свертывание яичных белков при варке яиц.
ДЕНАТУРАЦИЯ БЫВАЕТ ОБРАТИМОЙ И НЕОБРАТИМОЙ.
Необратимая денатурация может быть вызвана образованием нерастворимых веществ при действии на белки солей тяжелых металлов — свинца или ртути.
3. КАЧЕСТВЕННЫЕ РЕАКЦИИ НА БЕЛКИ:
1)Биуретовая реакция – фиолетовое окрашивание при действии на белки свежеосажденного гидроксида меди (II).
2) Ксантопротеиновая реакция — желтое окрашивание при действии на белки концентрированной азотной кислоты.
3) Реакция с щелочью в присутствии солей свинца – при нагревании выпадает черный осадок PbS, что свидетельствует о присутствии серосодержащих аминокислот.
Тематический тест на белки, жиры и углеводы.
Задание №1
Из предложенного списка соединений выберите те, которые можно обнаружить среди продуктов гидролиза природных жиров. Число верных ответов может быть любым.
1) этиленгликоль
2) серная кислота
3) глицерин
4) ацетон
5) стеариновая кислота
Решение
Ответ: 35
Задание №2
Из предложенного списка соединений выберите те, которые можно обнаружить среди продуктов гидролиза природных углеводов. Число верных ответов может быть любым.
1) глюкоза
2) аланин
3) фосфорная кислота
4) фруктоза
5) сорбит
Решение
Ответ: 14
Задание №3
Из предложенного списка соединений выберите те, которые можно обнаружить среди продуктов гидролиза природных белков. Число верных ответов может быть любым.
1) глицерин
2) анилин
3) олеиновая кислота
4) аланин
5) кофеин
Решение
Ответ: 4
Задание №4
Из предложенного списка соединений выберите те, которые нельзя обнаружить среди продуктов гидролиза природных жиров. Число верных ответов может быть любым.
1) олеиновая кислота
2) линолевая кислота
3) глицерин
4) бензойная кислота
5) пальмитиновая кислота
Решение
Ответ: 4
Задание №5
Из предложенного списка соединений выберите те, которые нельзя обнаружить среди продуктов гидролиза природных белков. Число верных ответов может быть любым.
1) глицин
2) глицерин
3) аланин
4) фенол
5) метиламин
Решение
Ответ: 245
Задание №6
Из предложенного списка функциональных групп выберите те, которые встречаются в моносахаридах. Число верных ответов может быть любым.
1) карбоксильная
2) карбонильная
3) гидроксильная
4) нитрогруппа
5) аминогруппа
Решение
Ответ: 23
Задание №7
Из предложенного списка функциональных групп выберите те, которые не встречаются в моносахаридах. Число верных ответов может быть любым.
1) гидроксильная
2) амидная
3) карбоксильная
4) аминогруппа
5) сложноэфирная
Решение
Ответ: 2345
Задание №8
Из предложенного списка функциональных групп выберите те, которые встречаются в природных аминокислотах. Число верных ответов может быть любым.
1) карбонильная
2) нитрогруппа
3) аминогруппа
4) карбоксильная
5) сложноэфирная
Решение
Ответ: 34
Задание №9
Из предложенного списка типов реакций выберите те, которые характерны для белков. Число верных ответов может быть любым.
1) кислотный гидролиз
2) денатурация
3) присоединение
4) щелочной гидролиз
5) полимеризация
Решение
Ответ: 124
Задание №10
Из предложенного списка типов реакций выберите те, которые характерны для моносахаридов и дисахаридов. Число верных ответов может быть любым.
1) этерификация
2) окисление
3) полимеризация
4) гидролиз
5) нитрование
Решение
Ответ: 12
[adsp-pro-3]
Задание №11
Из предложенного списка типов реакций выберите те, которые характерны для белков и дисахаридов. Число верных ответов может быть любым.
1) горение
2) кислотный гидролиз
3) спиртовое брожение
4) нитрование
5) гидратация
Решение
Ответ: 12
Задание №12
Из предложенного списка типов реакций выберите те, которые характерны для предельных жиров. Число верных ответов может быть любым.
1) гидрирование
2) горение
3) гидратация
4) обесцвечивание бромной воды
5) гидрогалогенирование
Решение
Ответ: 2
Задание №13
Из предложенного списка типов реакций выберите те, которые характерны для жидких жиров. Число верных ответов может быть любым.
1) полимеризация
2) обесцвечивание бромной воды
3) этерификация
4) омыление
5) брожение
Решение
Ответ: 124
Задание №14
Из предложенного списка типов реакций выберите те, которые характерны для твердых и жидких жиров. Число верных ответов может быть любым.
1) омыление
2) полимеризация
3) гидрирование
4) горение
5) нитрование
Решение
Ответ: 14
Задание №15
Из предложенного списка типов реакций выберите те, которые характерны для полисахаридов и твердых жиров. Число верных ответов может быть любым.
1) кислотный гидролиз
2) омыление
3) бромирование
4) реакция «серебряного зеркала»
5) горение
Решение
Ответ: 15
Задание №16
Из предложенного списка соединений выберите те, которые реагируют с глюкозой. Число верных ответов может быть любым.
1) аммиак
2) цинк
3) водород
4) гидроксид меди
5) вода
Решение
Ответ: 34
Задание №17
Из предложенного списка соединений выберите те, которые реагируют с сахарозой. Число верных ответов может быть любым.
1) кислород
2) водород
3) аммиачный раствор оксида серебра
4) никель
5) водный раствор серной кислоты
Решение
Ответ: 15
Задание №18
Из предложенного списка соединений выберите те, которые реагируют с рибозой. Число верных ответов может быть любым.
1) гидроксид натрия
2) гидроксид меди
3) водород
4) вода
5) мел
Решение
Ответ: 23
Задание №19
Из предложенного списка соединений выберите те, которые не реагируют с фруктозой. Число верных ответов может быть любым.
1) кислород
2) водород
3) гидроксид меди
4) аммиачный раствор оксид серебра
5) вода
Решение
Ответ: 45
Задание №20
Из предложенного списка соединений выберите те, которые реагируют с твердыми жирами. Число верных ответов может быть любым.
1) едкий натр
2) кремнезем
3) сероводород
4) гашеная известь
5) пирит
Решение
Ответ: 14
[adsp-pro-3]
Задание №21
Из предложенного списка соединений выберите те, которые реагируют с непредельными жирами. Число верных ответов может быть любым.
1) бромная вода
2) едкое кали
3) графит
4) водород
5) азот
Решение
Ответ: 124
Задание №22
Из предложенного списка соединений выберите те, которые не реагируют с дезоксирибозой. Число верных ответов может быть любым.
1) аргон
2) литий
3) кислород
4) аммиачный раствор оксида серебра
5) гидроксид меди
Решение
Ответ: 1
Задание №23
Из предложенного списка соединений выберите те, которые не реагируют с насыщенными жирами. Число верных ответов может быть любым.
1) бромная вода
2) гидроксид цезия
3) водород
4) гашеная известь
5) хлорид натрия
Решение
Ответ: 135
Задание №24
Из предложенного списка соединений выберите те, которые реагируют с белками. Число верных ответов может быть любым.
1) азотная кислота
2) кислород
3) водород
4) азот
5) железо
Решение
Ответ: 12
Задание №25
Из предложенного списка соединений выберите те, которые не реагируют с глюкозой. Число верных ответов может быть любым.
1) уксусный ангидрид
2) гидроксид меди
3) водород
4) перманганат калия
5) бромид калия
Решение
Ответ: 5
Задание №26
Из предложенного списка соединений выберите те, которые можно использовать для обнаружения глюкозы. Число верных ответов может быть любым.
- 1. [Ag(NH3)2]OH
- 2. NaCl
- 3. Zn
- 4. NaHCO3
- 5. Cu(OH)2
Решение
Ответ: 15
Задание №27
Из предложенного списка соединений выберите те, с помощью которых можно различить предельный и непредельный жиры. Число верных ответов может быть любым.
1) аммиак
2) калий
3) оксид кальция
4) бром
5) йод
Решение
Ответ: 45
Задание №28
Из предложенного списка соединений выберите те, с помощью которых можно различить рибозу и фруктозу. Число верных ответов может быть любым.
- 1. Сu(OH)2
- 2. FeO
- 3. FeCl3
- 4. Na
- 5. [Ag(NH3)2]OH
Решение
Ответ: 15
Задание №29
Из предложенного списка соединений выберите те, с помощью которых можно различить предельный жир и природный белок. Число верных ответов может быть любым.
1) бромная вода
2) азотная кислота
3) водород
4) кислород
5) серная кислота
Решение
Ответ: 2
Задание №30
Из предложенного списка соединений выберите те, с помощью которых можно различить непредельный жир и сахарозу. Число верных ответов может быть любым.
1) раствор брома
2) серная кислота
3) гидроксид меди
4) азот
5) оксид цинка
Решение
Ответ: 13
[adsp-pro-3]
Задание №31
Из предложенного списка соединений выберите те, с помощью которых можно различить предельный жир и глюкозу. Число верных ответов может быть любым.
- 1. [Ag(NH3)2]OH
- 2. I2
- 3. Zn
- 4. K2CO3
- 5. KMnO4
Решение
Ответ: 15
Задание №32
Из предложенного списка реагентов выберите два таких, с помощью которых можно различить природный белок и крахмал.
1) соляная кислота
2) раствор серной кислоты
3) азотная кислота
4) фосфор
5) йод
Решение
Ответ: 35
Задание №33
Из предложенного списка соединений выберите те, с помощью которых можно различить рибозу и глицин. Число верных ответов может быть любым.
1) аммиачный раствор оксида серебра
2) сода
3) ацетон
4) бензол
5) кислород
Решение
Ответ: 12
Задание №34
Из предложенного списка соединений выберите те, с помощью которых можно различить непредельный жир и целлюлозу. Число верных ответов может быть любым.
1) бромная вода
2) аммиак
3) алюминий
4) гидроксид натрия
5) вода
Решение
Ответ: 1
Задание №35
Из предложенного списка соединений выберите те, с помощью которых можно различить предельный жир и уксусную кислоту. Число верных ответов может быть любым.
1) серная кислота
2) азотная кислота
3) сода
4) водород
5) йод
Решение
Ответ: 3
Задание №36
Установите соответствие между природными соединениями и веществами, которые можно получить из них в одну стадию.
| ВЕЩЕСТВО | ПРОДУКТ |
|
А) глюкоза Б) сахароза В) растительное масло |
1) сорбит 2) глицин 3) фруктоза 4) маргарин |
Решение
Ответ: 134
Задание №37
Установите соответствие между природными соединениями и веществами, которые можно получить из них в одну стадию.
| ВЕЩЕСТВО | ПРОДУКТ |
|
А) твердый жир Б) крахмал В) целлюлоза |
1) ацетатное волокно 2) глюкоза 3) этиленгликоль 4) глицерин |
Решение
Ответ: 421
Задание №38
Установите соответствие между природными соединениями и веществами, которые можно получить из них в одну стадию.
| ВЕЩЕСТВО | ПРОДУКТ |
|
А) растительный белок Б) сахароза В) подсолнечное масло |
1) глюкоза 2) азот 3) рибоза 4) твердый жир |
Решение
Ответ: 214
Задание №39
Установите соответствие между природными соединениями и веществами, которые можно получить из них в одну стадию.
| ВЕЩЕСТВО | ПРОДУКТ |
|
А) глюкоза Б) бараний жир В) животный белок |
1) фруктоза 2) глицин 3) стеариновая кислота 4) этанол |
Решение
Ответ: 432
Задание №40
Установите соответствие между природными соединениями и веществами, которые можно получить из них в одну стадию.
| ВЕЩЕСТВО | ПРОДУКТ |
|
А) растительное масло Б) твердый жир В) гликоген |
1) глюкоза 2) маргарин 3) сорбит 4) мыло |
Решение
Ответ: 241
[adsp-pro-3]
Задание №41
Из предложенного перечня выберите два вещества, которые взаимодействуют и с глюкозой, и с целлюлозой.
1) водород
2) сульфат меди (II)
3) гидроксид железа (III)
4) азотная кислота
5) кислород
Решение
Ответ: 45
Задание №42
Из предложенного перечня выберите два вещества, которые не подвергаются гидролизу.
1) крахмал
2) целлюлоза
3) глюкоза
4) сахароза
5) фруктоза
Решение
Ответ: 35
Задание №43
Из предложенного перечня выберите две реакции, в которые не вступает целлюлоза.
1) горение
2) гидролиз
3) нитрование
4) хлорирование
5) гидрирование
Решение
Ответ: 45
Задание №44
Из предложенного перечня выберите два вещества, с которыми не реагирует крахмал.
1) йод
2) гидроксид меди (II)
3) аммиак
4) вода в присутствии кислот
5) вода в присутствии ферментов
Решение
Ответ: 23
Задание №45
Из предложенного перечня выберите два вещества, которые взаимодействуют с белками.
- 1. Cl2 (H2O)
- 2. HNO3
- 3. Ag2O (р-р NH3)
- 4. Cu(OH)2
- 5. FeCl3
Решение
Ответ: 24
[adsp-pro-10]
Видеоурок 1: Сложные эфиры. Жиры
Видеоурок 2: Белки
Видеоурок 3: Углеводы. Глюкоза
Лекция: Биологически важные вещества: жиры, белки, углеводы (моносахариды, дисахариды, полисахариды)

Жиры – это определенные органические соединения природного или синтетического происхождения. Представляют собой сложные эфиры глицерина и высших карбоновых кислот.
Данные вещества содержат в своей структуре остатки предельных карбоновых кислот. Формулы жиров можно представить в следующем виде:
Справа от формул изображена модель молекулы тристеарина, она иллюстрирует сложное строение жиров. Жиры по происхождению подразделяются на животные и растительные. Они отличаются своим составом, следовательно, и химическим свойствам.
Природные жиры животного происхождения являются твердыми веществами, за исключением рыбьего жира. Данный вид жиров содержит остатки предельных (насыщенных) карбоновых кислот, к примеру, стеариновой (C17H35COOH) или пальмитиновой (C15H31COOH). Жиры с кислотными остатками непредельных (ненасыщенных) карбоновых кислот, к примеру, олеиновой (C17H33COOH) или линолевой (C17H31COOH), содержатся в жидкой форме и считаются продуктами жизнедеятельности растений. В данном ряду также имеется и исключение — твердое пальмовое масло. Растительные жиры иначе именуют маслами.
Насыщение двойных связей в молекулах жидких жиров приводит к их отвердеванию. При гидрировании жидкого растительного масла на никелевом катализаторе появляется твердый жир, называемый маргарином. Уравнение данной реакции условно выглядит так:
Так как жиры представляют собой сложные эфиры, то, следовательно, они вступают в реакции гидролиза:
Данная реакция проходит под действием водных растворов кислот и щелочей. В случае применения щелочей, гидролиз проходит необратимо. При этом происходит образование глицерина и мыла (стеарат натрия):
Мыло — смесь натриевых или калиевых солей жирных карбоновых кислот.
Для жиров, содержащих в своей структуре кислотные остатки непредельных карбоновых кислот, присущи все качественные реакции на непредельные соединения. К таким относятся: обесцвечивание раствора перманганата калия и бромной воды. Предельные жиры в реакцию данного типа не вступают. Жир вступает в реакцию и с водным раствором перманганата калия и бромной водой. Это объясняется тем, что он содержит кислотные остатки непредельной карбоновой кислоты – олеиновой.

Белки — высокомолекулярные органические соединения, состоящие из остатков аминокислот, соединённых в длинную цепочку пептидной связью.
В состав белков живых организмов входит всего 20 типов аминокислот, все из которых относятся к альфа-аминокислотам, а аминокислотный состав белков и их порядок соединения друг с другом определяются индивидуальным генетическим кодом живого организма. Одной из особенностей белков является их способность самопроизвольно формировать пространственные структуры характерные только для данного конкретного белка.
Из-за специфики своего строения белки могут обладать разнообразными свойствами. Белки, имеющие глобулярную четвертичную структуру, в частности белок куриного яйца, растворяются в воде с образованием коллоидных растворов. Белки, обладающие фибриллярной четвертичной структурой, в воде не растворяются. Фибриллярными белками, в частности, образованы ногти, волосы, хрящи.
Химические свойства белков:
-
Гидролиз. Все белки способны вступать в реакцию гидролиза. В случае полного гидролиза белков образуется смесь из α-аминокислот:
-
Денатурация. Разрушение вторичной, третичной и четвертичной структур белка без разрушения его первичной структуры называют денатурацией. Денатурация белка может протекать под действием растворов солей натрия, калия или аммония – такая денатурация является обратимой. Денатурация же протекающая под действием излучения (например, нагрева) или обработке белка солями тяжелых металлов является необратимой. Необратимая денатурация белка наблюдается при термической обработке яиц в процессе их приготовления. В результате денатурации яичного белка его способность растворяться в воде с образованием коллоидного раствора исчезает.
Качественные реакции на белки:
-
Биуретовая реакция. Если к раствору, содержащему белок добавить 10%-й раствор гидроксида натрия, а затем небольшое количество 1 %-го раствора сульфата меди, то появится фиолетовое окрашивание. Раствор белка + NаОН(10%-ный р-р) + СuSO4 = фиолетовое окрашивание.
-
Ксантопротеиновая реакция. Растворы белка при кипячении с концентрированной азотной кислотой окрашиваются в желтый цвет. Раствор белка + HNO3(конц.) => желтое окрашивание.
Биологические функции белков:
-
Каталитическая. Ускоряет различные химические реакции в живых организмах.
-
Структурная. Строительные материалы клеток. Ферменты: коллаген, белки клеточных мембран.
-
Защитная. Защищают организм от инфекций. Ферменты: иммуноглобулины, интерферон.
-
Регуляторная. Регулируют обменные процессы. Ферменты: гормоны.
-
Транспортная. Перенос жизненно-необходимых веществ от одних частей организма к другим. Ферменты: гемоглобин переносит кислород.
-
Энергетическая. Снабжает организм энергией. Ферменты: 1 грамм белка может обеспечить организм энергией в количестве 17,6 Дж.
-
Моторная (двигательная). Ферменты: миозин (мышечный белок).

Углеводы — органические соединения, состоящие из молекул углерода, водорода и кислорода, общая формула которых Cn(H2O)m.
Из формулы углеводов можно предположить то, что данные соединения состоят из углерода и воды, однако это не так, просто соотношение водорода и кислорода в данных соединениях такое же, как и у воды 2:1. Однако следует иметь ввиду, что данное соотношение водорода и кислорода в углеводах непостоянно, к примеру, дезоксирибоза имеет формулу С5Н10О4. Также существуют соединения соответстсвующие формуле Cn(H2O)m, но к углеводам не относящиеся. Это формальдегид (СН2О) и уксусная кислота (С2Н4О2).
Рассмотрим классификацию углеводов. В её основе лежит способность одних углеводных соединений при гидролизе расщепляться на углеводы меньшей молекулярной массы. Исходя из этого, углеводы делят на:
-
простые (моносахариды) и
-
сложные (дисахариды, полисахариды).
Моносахариды не расщепляются, т.е. не гидролизуются. В зависимости от числа атомов они делятся на триозы, тетрозы, пентозы, гексозы и т.д. Среди них широко распространены в природе пентозы с общей формулой C5(H2O)5 и гексозы C6H12O6. Например, среди пентозов, известные вам из курса биологии рибоза C5H10O5 и дезоксирибоза C5H10O4, входящие в состав РНК и ДНК. Среди гексозов: глюкоза, фруктоза, галактоза, имеющие общую формулу C6H12O6. Общей чертой глюкозы и фруктозы является наличие в составе молекул пяти гидроксильных групп. Поэтому они считаются многоатомными спиртами. Отличие состоит в том, что молекула глюкозы содержит альдегидную группу (-CHO), а молекула фруктозы кетонную группу (R—CO—R’). Таким образом, глюкоза — это многоатомный альдегидоспирт, фруктоза – многоатомный кетоспирт.
Строение молекул глюкозы и фруктозы:
Дисахариды при гидролизе расщепляются на две молекулы моносахаридов. Исходя из общей формулы большинства дисахаридов C12H22O11 уравнение гидролиза выглядит так:
- C12H22O11 + H2O → 2C6H12O6 (образовалось две молекулы гексозы).
К дисахаридам относятся: сахароза, распадающаяся при гидролизе на молекулу глюкозы и молекулу фруктозы; мальтоза, распадающаяся при гидролизе на две молекулы глюкозы; лактоза, распадающаяся при гидролизе на молекулу глюкозы и молекулу галактозы. Наиболее часто встречается сахароза. Её молекула образована циклическими остатками одной молекулы глюкозы и одной молекулы фруктозы:
Полисахариды при полном гидролизе образуют множество моносахаридов, чаще всего глюкозы. К данной группе углеводов относятся: крахмал, гликоген, целлюлоза, хитин и др. Структура молекулы крахмала:

Химические свойства моносахаридов:
1. Гидрирование, т.е. взаимодействие с водородом при помощи катализаторов:
- глюкоза: С6Н12О6 + Н2 → С6Н14О6 (образовался шестиатомный спирт сорбит);
- фруктоза С6Н12О6 + Н2 → C6H14O6 + C6H14O6 (образовалась изомерная смесь сорбита и маннита)
2. Качественные реакции глюкозы как альдегида:
-
глюкоза с гидроксидом меди (II): СН2ОН – (СНОН)4 – СОН + Сu(ОН)2 → СН2ОН – (СНОН)4 – СООН + Сu2О↓+ Н2О
-
реакция «серебряного зеркала»: HCOOH + 2[Ag(NH3)2]OH → CO2↑ + 2Ag↓ + 2H2O + 4NH3↑
В первой реакции наблюдается выпадение кирпично-красного осадка оксида меди (I). Альдегидная группа глюкозы окисляется до карбоксильной – образуется глюконовая кислота. Во второй реакции вместо глюконовой кислоты образуется ее соль – глюконат аммония, т.к. в растворе присутствует растворенный аммиак. Данные реакции из моносахаридов свойственны только глюкозе.
3. Реакции брожения:
- спиртовое брожение: С6Н12О6 → 2С2Н5ОН + 2СО2 (этиловый спирт и углекислый газ);
- молочнокислое брожение: С6Н12О6 → 2СН3-СН(ОН)-СООН (молочная кислота).
Химические свойства дисахаридов:
1. Качественные реакции дисахаридов, как альдегидов. Одни дисахариды дают качественные реакции и альдегидную группу, а другие нет. К примеру, для сахарозы такие реакции невозможны, поскольку связь в её молекулах образована при конденсации двух ацетальных гидроксилов, а значит не может быть раскрытия ни одного из циклов, необходимого для перехода в карбонильную форму. Подобного рода дисахариды называют невосстанавливающими сахарами. Если в молекуле дисахарида остался полуацетальный гидроксил из альдегидной группы одной из исходных молекул моносахаридов, то качественные реакции на альдегиды возможны. В частности, мальтоза — восстанавливающий дисахарад, схожий по своим химическим свойствам с глюкозой:
-
мальтоза с гидроксидом меди (II):
(образовалась мальтоновая кислота);
- реакция «серебряного зеркала» (окисление мальтозы):
2. Гидролиз. Данный вид реакций свойствен всем дисахаридам. Проводится реакция в присутствии минеральных кислот (Н2SO4, НСl, Н2СО3). К примеру, гидролиз сахарозы приводит к образованию равных количеств глюкозы и фруктозы:
-
C12H22O11 + H2O → C6H12O6 + C6H12O6
Химические свойства полисахаридов:
1. Горение. Все полисахариды, в том числе крахмал и целлюлоза, при полном сгорании в кислороде образуют углекислый газ и воду:
-
(C6H10O5)n + 6nO2 → 6nCO2 + 5nH2O.
2. Гидролиз. При полном гидролизе крахмала или целлюлозы образуется один и тот же моносахарид – глюкоза:
- (C6H10O5)n + nH2O → nC6H12O6
3. Реакция этерификации с образованием сложных эфиров:
-
(C6H7O2(OH)3)n + 3nCH3COOH → (C6H7O2(OCOCH3)3)n + nH2O.
4. Качественная реакция на крахмал. При действии на что-либо, в чем содержится крахмал, появляется синее окрашивание. При нагревании синяя окраска исчезает, при охлаждении появляется вновь.
Биологически важные вещества: белки, жиры, углеводы
К белкам относят полипептиды, содержащие в своём составе больше 100 аминокислотных остатков. Их молекулярная масса лежит в пределах от 10 000 до нескольких миллионов.
В соответствии с числом аминокислотных остатков пептиды делят на олигопептиды и полипептиды. В состав олигопептидов (низкомолекулярных пептидов) входит не более 10 аминокислотных остатков. В состав цепи полипептидов входит от 10 до 100 аминокислотных остатков.
По химическому составу белки делят на протеины, т. е. белки, при гидролизе которых образуются только аминокислоты (простые белки), и протеиды, т. е. соединения, при гидролизе которых, кроме аминокислот, выделяются и другие компоненты. Эта неаминокислотная часть сложного белка называется простетической группой.
По форме молекул различают глобулярные (шаровидные) и фибриллярные (нитевидные) белки.
К глобулярным белкам относят альбумины и глобулины (широко распространённые в органах и тканях организма), а к фибриллярным — коллаген (основной белок соединительной ткани).
Последовательность аминокислотных звеньев в линейной полипептидной цепи называют первичной структурой белка.
Вторичной структурой белка называют форму полипептидной цепи в пространстве. Вторичная структура определяется тем, что из-за образования внутримолекулярных водородных связей макромолекулы принимают определённую конформацию. Часто вторичная структура представляет собой спираль.
Третичная структура определяется пространственным расположением макромолекулы как целого и зависит, например, от взаимодействия полярных и неполярных заместителей в разных местах цепи, от образования S–S-связей между противоположными цистеиновыми остатками.
Четвертичной структурой белка называют сложные образования из отдельных молекул белка.
Денатурацией белка называют процесс потери им его естественных свойств. Денатурация происходит под действием высоких температур или активных химических веществ, при этом происходит нарушение всех структур белковой молекулы, за исключением первичной.
Жирами называют смесь сложных эфиров глицерина и высших карбоновых кислот. При этом в состав жиров могут входить самые разнообразные высшие жирные кислоты, но только один спирт — глицерин. Поэтому эти эфиры называют глицеридами. Общая формула жиров:
где R, R1, R2 — углеводородные остатки.
В состав твёрдых жиров входят предельные кислоты: C15H31COOH — пальмитиновая кислота; C17H35COOH — стеариновая кислота.
Жиры, триглицериды которых состоят одновременно из насыщенных и ненасыщенных кислот, широко встречаются в природе.
Жидкие жиры часто называют маслами. Глицериды насыщенных кислот — твёрдые соединения, а ненасыщенных — жидкие. Растительные масла, в состав которых входят непредельные кислоты, чаще всего — жидкие продукты.
Наиболее важными химическими свойствами жиров является их способность к гидролизу и гидрогенизации. Гидролиз жиров происходит в кислой или щелочной среде при повышенной температуре. При гидролизе щёлочью образуются глицерин и соли высших кислот — мыла, отсюда и происходит название этого процесса — омыление:
В присутствии мелкораздробленного никеля происходит присоединение водорода по двойным связям ненасыщенных кислот. При этом жидкие растительные масла переходят в твёрдые.
Углеводами называют класс соединений, отвечающих общей формуле Cn(H2O)m. Известны также некоторые вещества, проявляющие свойства углеводов, но формально не отвечающие общей формуле.
Углеводы широко распространены в природе и играют важную роль в жизни человека, животных и растений. Они являются одним из основных продуктов питания.
Название «углеводы» — историческое. Первые из изученных представителей этого класса соединений соответствовали формуле Cn(H2O)m и формально рассматривались как гидраты углерода. Хотя данная формула справедлива для многих представителей углеводов, их строение не соответствует «гидратам углерода».
Углеводы делят на две группы: моносахариды и полисахариды. Моносахариды при гидролизе не способны распадаться на более простые углеводы. Полисахаридами называют углеводы, способные подвергаться гидролизу с образованием моносахаридов.
Наиболее распространёнными среди моносахаридов являются глюкоза и фруктоза. Эти вещества являются изомерами и имеют формулу C6H12O6.
Глюкоза широко распространена в природе, в свободном состоянии встречается во фруктах, меде и т. д. Используется в пищевой промышленности, медицине. В промышленности глюкозу получают из крахмала кипячением с разбавленной серной кислотой.
Фруктоза хорошо растворима в воде, встречается в свободном виде во многих фруктах и плодах. Является ценным питательным продуктом. Она в три раза слаще глюкозы.
Сахароза C12H22O11 относится к дисахаридам.
При гидролизе сахарозы образуются глюкоза и фруктоза:
Смесь равных количеств глюкозы и фруктозы, образующаяся при гидролизе сахарозы, называют инвертным сахаром. Сахароза содержится в сахарном тростнике, сахарной свёкле и кукурузе. Она является важным пищевым продуктом.
























![[[pictureof]]](https://dist-tutor.info/s3/dist-tutor/user/20094/ava/thumbnails/mQ6siSVtAT1Szar.jpg)