Жиры – это сложные эфиры, образованные глицерином и высшими одноосновными карбоновыми кислотами (жирными кислотами).
.
Жиры образуются при взаимодействии глицерина и высших карбоновых кислот:
| Жирные (высшие) кислоты | |
| Предельные кислоты | Непредельные кислоты |
| Масляная кислота С3Н7 -СООН | Олеиновая кислота С17Н33СООН
(содержит одну двойную связь в радикале) СН3—(СН2)7—СН = СН—(СН2)7—СООН |
| Пальмитиновая кислота С15Н31 — СООН | Линолевая кислота С17Н31СООН
(две двойные связи в радикале) |
| Стеариновая кислота С17Н35 — СООН | Линоленовая кислота С17Н29СООН
(три двойные связи в радикале) СН3СН2СН=CHCH2CH=CHCH2CH=СН(СН2)4СООН |
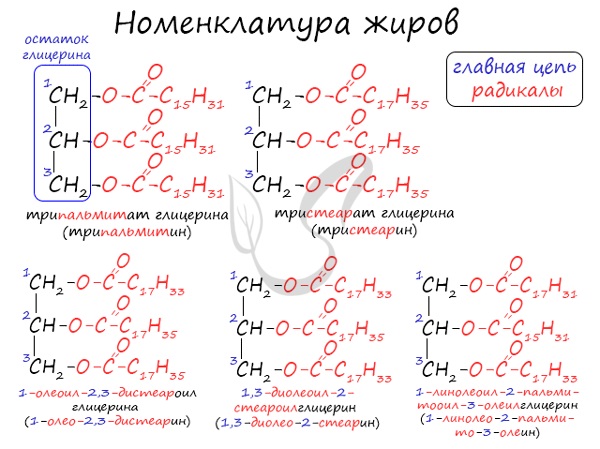
Номенклатура жиров
Общее название жиров – триацилглицерины (триглицериды).
Существует несколько способов назвать молекулу жира.
Например, жир, образованный тремя остатками стеариновой кислоты, будет иметь следующие названия:
Физические свойства жиров
Жиры растворимы в органических растворителях и нерастворимы в воде. С водой жиры не смешиваются.
| Животные жиры — предельные | Растительные жиры (масла) — непредельные |
| Твёрдые, образованы предельными кислотами – стеариновой и пальмитиновой.
Все животные жиры, кроме рыбьего – твёрдые. |
Жидкие, образованы непредельными кислотами – олеиновой, линолевой и другими.
Все растительные жиры, кроме пальмового масла – жидкие. |
Химические свойства жиров
1. Гидролиз (омыление) жиров
Жиры подвергаются гидролизу в кислой или щелочной среде или под действием ферментов.
1.1. Кислотный гидролиз
Под действием кислот жиры гидролизуются до глицерина и карбоновых кислот, которых входили в молекулу жира.
Например, при гидролизе тристеарата глицерина в кислой среде образуется стеариновая кислота и глицерин
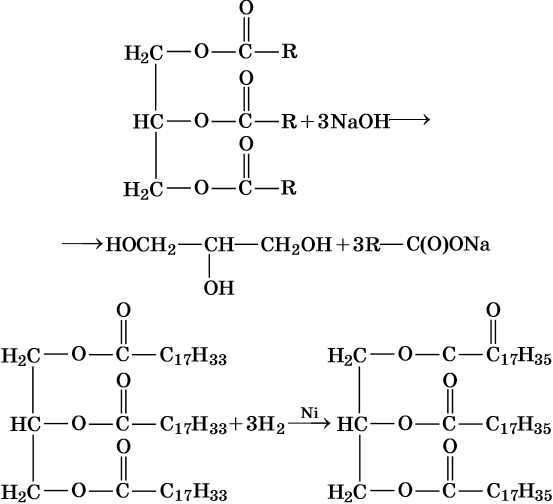
1.2. Щелочной гидролиз — омыление жиров
При щелочном гидролизе жиров образуется глицерин и соли карбоновых кислот, входивших в состав жира.
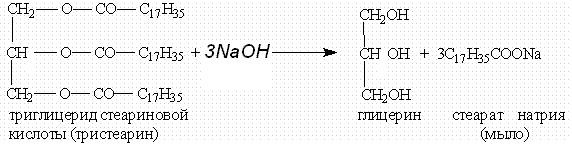
Например, при гидролизе тристеарата глицерина гидроксидом натрия образуется стеарат натрия.
2. Гидрирование (гидрогенизация) ненасыщенных жиров
Гидрогенизация жиров — это процесс присоединения водорода к остаткам непредельных кислот, входящих в состав жира.
При этом остатки непредельных кислот переходят в остатки предельных, жидкие растительные жиры превращаются в твёрдые (маргарин).
Например, триолеат глицерина при гидрировании превращается в тристеарат глицерина:
Количественной характеристикой степени ненасыщенности жиров служит йодное число, показывающее, какая масса йода может присоединиться по двойным связям к 100 г жира.
3. Мыло и синтетические моющие средства
При щелочном гидролизе жиров образуются мыла – соли высших жирных кислот.
Стеарат натрия – твёрдое мыло.
Стеарат калия – жидкое мыло.
Моющая способность мыла зависит от жесткости воды. Оно хорошо мылится и стирает в мягкой воде, плохо стирает в жёсткой воде и совсем не стирает в морской воде, так как содержащие в ней ионы Ca2+ и Mg2+ образуют с высшими кислотами нерастворимые в воде соли.
Например, стеарат глицерина взаимодействует с сульфатом кальция
Поэтому наряду с мылом используют синтетические моющие средства.
Их производят из других веществ, например из алкилсульфатов — солей сложных эфиров высших спиртов и серной кислоты.
Спирт реагирует с серной кислотой с образованием алкилсульфата.
Далее алкилсульфат гидролизуется щелочью:
Эти соли содержат в молекуле от 12 до 14 углеродных атомов и обладают очень хорошими моющими свойствами. Кальциевые и магниевые соли этих веществ растворимы в воде, а потому такие мыла моют и в жесткой воде. Алкилсульфаты содержатся во многих стиральных порошках.
Жиры — органические соединения, по строению являющиеся сложными эфирами трехатомного спирта глицерина и высших карбоновых (жирных)
кислот.
К жирным кислотам (их формулы лучше выучить 
- Пальмитиновая — C15H31COOH (предельная)
- Стеариновая — C17H35COOH (предельная)
- Олеиновая — C17H33COOH (непредельная, 1 двойная связь в радикале)
- Линолевая — C17H31COOH (непредельная, 2 двойные связи в радикале)
- Линоленовая — C17H29COOH (непредельная, 3 двойные связи в радикале)
Растительные и животные жиры
Жиры образуются в организме растений и животных, служат запасным питательным веществом. В строении растительных и животных жиров
есть некоторые важные отличия.
Заметьте, что растительные жиры чаще жидкие и в них входят преимущественно остатки непредельных жирных кислот, а животные жиры — твердые и
содержат остатки предельных жирных кислот.

Номенклатура жиров
По систематической номенклатуре жиры принято называть триацилглицеринами. Названия жирам дают в зависимости от ацилов — остатков жирных
кислот, входящих в их состав. Для формирования единого названия к остаткам кислот добавляют суффикс «оил».
В соответствии с тривиальной номенклатурой, жиры называют, добавляя окончание «ин» к названию кислоты и приставку, указывая, сколько гидроксогрупп
в молекуле глицерина подверглось этерификации. В общем лучше 1 раз увидеть, чем 100 раз услышать 
Получение жиров
Жиры (по строению сложные эфиры) получаются в реакции этерификации, протекающей между трехатомным спиртом глицерином и высшими карбоновыми
(жирными) кислотами.
В зависимости от того, какие именно кислоты участвуют в реакции, образуются различные жиры.

Химические свойства жиров
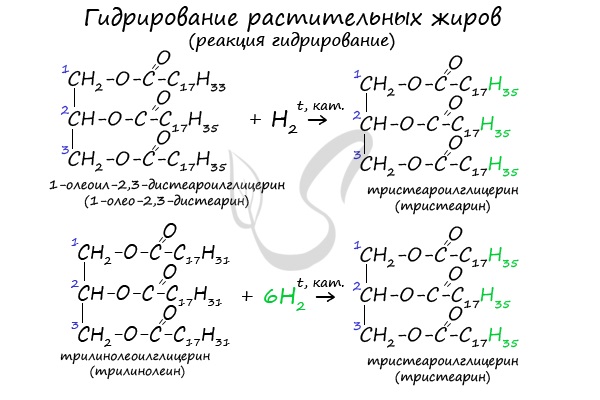
- Гидрирование растительных жиров
- Гидролиз
В состав растительных жиров входят непредельные кислоты, которые поддаются гидрированию и превращаются в предельные. Таким путем в пищевой
промышленности получают маргарин.
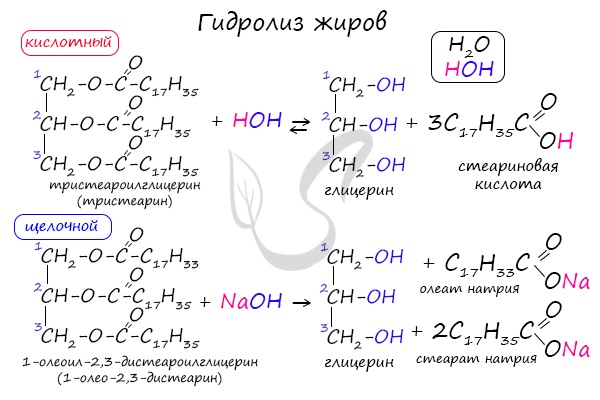
Как сложные эфиры, жиры способны вступать в реакцию гидролиза, который может быть кислотным и щелочным. В результате кислотного гидролиза
образуется глицерин и исходные жирные кислоты, в результате щелочного гидролиза — глицерин и соли жирных кислот.
Реакция щелочного гидролиза жиров называется реакцией омыления, в результате получаются соли жирных кислот — мыла. Кислотный гидролиз протекает
обратимо, щелочной — необратимо.
В состав твердого мыла входят соли Na, в состав жидкого — K.
© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
3.8.1. Жиры.
Жиры – органические соединения природного или синтетического происхождения, представляющие собой продукты полной этерификации глицерина карбоновыми кислотами.
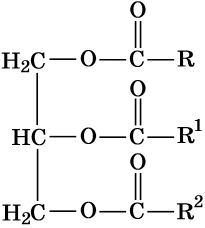
Т.е. общую формулу жиров можно записать как:
где R1,R2 и R3 – одинаковые либо различные углеводородные радикалы с числом углеродных атомов более 2-х, имеющие неразветвленный углеродный скелет и разную степень насыщенности.
В жирах природного происхождения наиболее часто встречаются следующие кислотные остатки:
| Название жирной кислоты | Формула | Количество C=C связей в молекуле |
| Масляная | C3H7COOH | — |
| Капроновая | C5H11COOH | — |
| Пальмитиновая | C15H31COOH | — |
| Стеариновая | C17H35COOH | — |
| Олеиновая | C17H33COOH | 1 |
| Линолевая | C17H31COOH | 2 |
| Линоленовая | C17H29COOH | 3 |
Следует отметить, что жиры, содержащие в своей структуре только остатки предельных карбоновых кислот, являются твердыми веществами, а жиры с кислотными остатками непредельных кислот – жидкие. Большинство жиров животного происхождения являются твердыми веществами, исключением является жидкий рыбий жир. В свою очередь большинство жидких жиров являются продуктами жизнедеятельности растений, исключение – твердое пальмовое масло. Растительные жиры также называют маслами.
Логично предположить, что поскольку жидкие жиры состоят из глицерина и кислотных остатков непредельных кислот, а твердые – предельных, то насыщение двойных связей в молекулах жидких жиров должно приводить к их отвердеванию. И действительно, при гидрировании жидкого растительного масла на никелевом катализаторе (никеле Ренея) образуется твердый жир, который носит название маргарин:
Поскольку жиры представляют собой сложные эфиры, то они вступают в реакции гидролиза под действием водных растворов кислот и щелочей. В случае гидролиза под действием кислот уравнение гидролиза имеет вид:
В случае использования щелочей гидролиз протекает необратимо с образованием глицерина и мыла. Мылом называют смеси натриевых или калиевых солей жирных карбоновых кислот:
Для жиров, содержащих в своей структуре кислотные остатки непредельных карбоновых кислот, очевидно, характерны все качественные реакции на непредельные соединения, а именно – обесцвечивание ими раствора перманганата калия и бромной воды. Предельные жиры в такую реакцию не вступают.
Так, например, жир, представляющий собой триолеат глицерина, вступает в реакцию и с водным раствором перманганата калия и бромной водой, поскольку содержит кислотные остатки непредельной карбоновой кислоты – олеиновой. Напротив, трипальмитат глицерина в подобные реакции не вступает, т.к. не содержит кратных (двойных) углерод-углеродных связей.
Чтобы поделиться, нажимайте
Сложные эфиры – функциональные производные карбоновых кислот,
в молекулах которых гидроксильная группа (-ОН) замещена на остаток спирта (-OR)
Сложные эфиры карбоновых кислот – соединения с общей формулой
R–COOR’, где R и R’ – углеводородные радикалы.
Физические свойства:
- · Летучие, бесцветные жидкости
- · Плохо растворимы в воде
- · Чаще с приятным запахом
- · Легче воды
Сложные эфиры содержатся в цветах, фруктах, ягодах. Они определяют их специфический запах.
Являются составной частью эфирных масел (известно около 3000 эф.м. – апельсиновое, лавандовое, розовое и т. д.)
Эфиры низших карбоновых кислот и низших одноатомных спиртов имеют приятный запах цветов, ягод и фруктов. Эфиры высших одноосновных кислот и высших одноатомных спиртов – основа природных восков. Например, пчелиный воск содержит сложный эфир пальмитиновой кислоты и мирицилового спирта (мирицилпальмитат):
CH3(CH2)14–CO–O–(CH2)29CH3
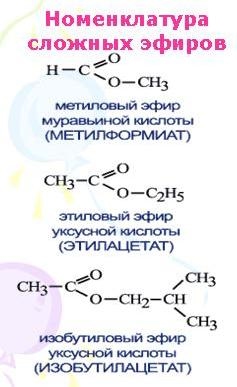
Краткие названия сложных эфиров строятся по названию радикала (R’) в остатке спирта и названию группы RCOO— в остатке кислоты. Например, этиловый эфир уксусной кислоты CH3COOC2H5 называется этилацетат.
Применение
· В качестве отдушек и усилителей запаха в пищевой и парфюмерной (изготовление мыла, духов, кремов) промышленности;
· В производстве пластмасс, резины в качестве пластификаторов.
Пластификаторы – вещества, которые вводят в состав полимерных материалов для придания (или повышения) эластичности и (или) пластичности при переработке и эксплуатации.
Применение в медицине
В конце XIX — начале ХХ века, когда органический синтез делал свои первые шаги, было синтезировано и испытано фармакологами множество сложных эфиров. Они стали основой таких лекарственных средств, как салол, валидол и др. Как местнораздражающее и обезболивающее средство широко использовался метилсалицилат, в настоящее время практически вытесненный более эффективными средствами.
Получение сложных эфиров
Cложные эфиры могут быть получены при взаимодействии карбоновых кислот со спиртами (реакция этерификации). Катализаторами являются минеральные кислоты.
Реакция этерификации в условиях кислотного катализа обратима. Обратный процесс – расщепление сложного эфира при действии воды с образованием карбоновой кислоты и спирта – называют гидролизом сложного эфира.
RCOOR’ + H2O (H+)↔ RCOOH + R’OH
Гидролиз в присутствии щелочи протекает необратимо (т.к. образующийся отрицательно заряженный карбоксилат-анион RCOO– не вступает в реакцию с нуклеофильным реагентом – спиртом).
Эта реакция называется омылением сложных эфиров (по аналогии со щелочным гидролизом сложноэфирных связей в жирах при получении мыла).
Жиры
Жиры — сложные эфиры глицерина и высших одноатомных карбоновых кислот .
Общее название таких соединений — триглицериды или триацилглицерины, где ацил — остаток карбоновой кислоты -C(O)R.
В состав природных триглицеридов входят остатки насыщенных кислот (пальмитиновой C15H31COOH, стеариновой C17H35COOH) и ненасыщенных (олеиновой C17H33COOH, линолевой C17H29COOH).
Жиры содержатся во всех растениях и животных. Животные жиры (бараний, свиной, говяжий и т.п.), как правило, являются твердыми веществами с невысокой температурой плавления (исключение — рыбий жир). Они состоят главным образом из триглицеридов предельных кислот.
Растительные жиры (подсолнечное масло, соевое, хлопковое и др.) – жидкости (исключение — кокосовое масло). В состав этих триглицеридов входят остатки непредельных кислот.
Жидкие жиры превращают в твердые путем реакции гидрогенизации (гидрирования). При этом водород присоединяется по двойной связи, содержащейся в углеводородном радикале молекул масел .
Продукт гидрогенизации масел — твердый жир (искусственное сало, саломас).
Маргарин — пищевой жир, состоит из смеси гидрогенизированных масел (подсолнечного, кукурузного, хлопкого и др.), животных жиров, молока и вкусовых добавок (соли, сахара, витаминов и др.).
Жирам как сложным эфирам свойственна обратимая реакция гидролиза, катализируемая минеральными кислотами. При участии щелочей гидролиз жиров происходит необратимо. Продуктами в этом случае являются мыла – соли высших карбоновых кислот и щелочных металлов.
Натриевые соли — твердые мыла, калиевые — жидкие. Реакция щелочного гидролиза жиров, и вообще всех сложных эфиров, называется также омылением.
Природные жиры содержат следующие жирные кислоты
| Насыщенные:
стеариновая (C17H35COOH) пальмитиновая (C15H31COOH) Масляная (C3H7COOH) |
В СОСТАВЕ
ЖИВОТНЫХ ЖИРОВ |
| Ненасыщенные:
олеиновая (C17H33COOH, 1 двойная связь) линолевая (C17H31COOH, 2 двойные связи) линоленовая (C17H29COOH, 3 двойные связи) арахидоновая (C19H31COOH, 4 двойные связи, реже встречается) |
В СОСТАВЕ
РАСТИТЕЛЬНЫХ ЖИРОВ |
Жиры содержатся во всех растениях и животных. Они представляют собой смеси полных сложных эфиров глицерина и не имеют чётко выраженной температуры плавления.
Физические свойства жиров
- Животные жиры (бараний, свиной, говяжий и т.п.), как правило, являются твердыми веществами с невысокой температурой плавления (исключение – рыбий жир). В твёрдых жирах преобладают остатки насыщенных кислот.
- Растительные жиры – масла (подсолнечное, соевое, хлопковое и др.) – жидкости (исключение – кокосовое масло, масло какао-бобов). Масла содержат в основном остатки ненасыщенных (непредельных) кислот.
Химические свойства жиров
1. Гидролиз, или омыление, жиров происходит под действием воды, с участием ферментов или кислотных катализаторов (обратимо) , при этом образуются спирт — глицерин и смесь карбоновых кислот:
или щелочей (необратимо). При щелочном гидролизе образуются соли высших жирных кислот, называемые мылами. Мыла получаются при гидролизе жиров в присутствии щелочей:
Мыла — это калиевые и натриевые соли высших карбоновых кислот.
2.Гидрирование жиров – превращение жидких растительных масел в твердые жиры – имеет большое значение для пищевых целей. Продукт гидрогенизации масел – твердый жир (искусственное сало, саломас). Маргарин – пищевой жир, состоит из смеси гидрогенизированных масел (подсолнечного, кукурузного, хлопкого и др.), животных жиров, молока и вкусовых добавок (соли, сахара, витаминов и др.).
Так в промышленности получают маргарин:
В условиях процесса гидрогенизации масел (высокая температура, металлический катализатор) происходит изомеризация части кислотных остатков, содержащих цис-связи С=С, в более устойчивые транс-изомеры. Повышенное содержание в маргарине (особенно, в дешевых сортах) остатков транс-ненасыщенных кислот увеличивает опасность атеросклероза, сердечно-сосудистых и других заболеваний.
Реакция получения жиров (этерификация)
Применение жиров
-
- Пищевая промышленность
-
- Фармацевтика
-
- Производство мыла и косметических изделий
-
- Производство смазочных материалов
ЕГЭ 2018 по химии › Подготовка к ЕГЭ 2018
Жиры
Жирами называют сложные эфиры глицерина и высших карбоновых кислот общей формулы:
где R, R1, R2 — углеводородные остатки.
Жиры встречаются в природе как соединения, образующиеся в процессе обмена веществ. Существуют жиры животного и растительного происхождения.
Ниже приведены формулы и тривиальные названия наиболее важных карбоновых кислот, входящих в состав жиров:
Характерные химические свойства жиров — реакции гидролиза в кислой или щелочной среде и реакции гидрогенизации:
Углеводы →
← Простые и сложные эфиры
- Курс
Меня зовут Быстрицкая Вера Васильевна.
Я репетитор по Химии
Вам нужны консультации по Химии по Skype?
Если да, подайте заявку. Стоимость договорная.
Чтобы закрыть это окно, нажмите «Нет».
Жиры — сложные эфиры глицерина и высших одноосновных карбоновых кислот (так называемых ЖИРНЫХ кислот).
Общее название таких соединений – триглицериды или триацилглицерины, где ацил – остаток карбоновой кислоты
ФИЗИЧЕСКИЕ СВОЙСТВА
Жидкие или твердые вещества, растворимые в органических растворителях, но не растворимые в воде.
ХИМИЧЕСКИЕ СВОЙСТВА.
ГИДРОЛИЗ ЖИРОВ
проходит в кислой или в щелочной среде, или под действием ферментов:
а) кислотный (водный) гидролиз:
под действием кислоты жиры гидролизуются до глицерина и карбоновых кислот, которых входили в молекулу жира.
б) щелочной гидролиз – омыление.
Получают глицерин и соли карбоновых кислот (мыла), входивших в состав жира. Мыла – соли высших жирных кислот (натриевые – твёрдые, калиевые – жидкие).
При пищеварении жир омыляется (расщепляется) с помощью ферментов.
ГИДРИРОВАНИЕ (ГИДРОГЕНИЗАЦИЯ)
процесс присоединения водорода к остаткам непредельных кислот, входящих в состав жира.
Остатки непредельных кислот переходят в остатки предельных, жидкие растительные жиры превращаются в твёрдые (маргарин).
Жидкие жиры обесцвечивают бромную воду, что говорит о наличии двойных связей
УГЛЕВОДЫ (САХАРА) — органические соединения, имеющие сходное строение и свойства, состав большинства которых отражает формула Cx(H2O)y, где x, y ≥ 3.
Исключение составляет дезоксирибоза, которая имеют формулу С5Н10O4.
МОНОСАХАРИДЫ — гетерофункциональные соединения, в состав их молекул входит одна карбонильная группа (альдегидная или кетонная) и несколько гидроксильных.
ФИЗИЧЕСКИЕ СВОЙСТВА МОНОСАХАРИДОВ
Моносахариды – твердые вещества, легко растворимые в воде, плохо – в спирте и совсем нерастворимые в эфире.
Водные растворы имеют нейтральную реакцию на лакмус.
Большинство моносахаридов обладают сладким вкусом, однако меньшим, чем свекловичный сахар.
ХИМИЧЕСКИЕ СВОЙСТВА МОНОСАХАРИДОВ
В водном растворе глюкозы существует динамическое равновесие между двумя циклическими формами — α и β и линейной формой:
СВОЙСТВА ГЛЮКОЗЫ, КАК МНОГОАТОМНОГО СПИРТА
1. Реакция комплексообразование с гидроксидом меди (II).
При взаимодействии свежеосажденного гидроксида меди (II) с моносахаридами происходит растворение гидроксида с образованием комплекса синего цвета.
2. Глюкоза, как альдегид.
Образование сложных эфиров с ангидридами кислот или галогенангидридами.
3. Реакция с гидроксидом меди (II) при нагревании
4. Окисление бромной водой до глюконовой кислоты.
4. Каталитическое гидрирование (восстановление) глюкозы
происходит восстановление карбонильной группы до спиртового гидроксила, получается шестиатомный спирт – сорбит.
5. РЕАКЦИИ БРОЖЕНИЯ.
а) спиртовое брожение
б) молочнокислое брожение
в) маслянокислое брожение
ФРУКТОЗА— структурный изомер глюкозы — КЕТОНОСПИРТ:
Кристаллическое вещество, хорошо растворимое в воде, более сладкое, чем глюкоза. В свободном виде содержится в мёде и фруктах.
Химические свойства фруктозы обусловлены наличием кетонной и пяти гидроксильных групп. При гидрировании фруктозы также получается СОРБИТ.
СВОЙСТВА ДИСАХАРИДОВ
это углеводы, молекулы которых состоят из двух остатков моносахаридов, соединенных друг с другом за счет взаимодействия гидроксильных групп (двух полуацетальных или одной полуацетальной и одной спиртовой).
1. САХАРОЗА (СВЕКЛОВИЧНЫЙ ИЛИ ТРОСТНИКОВЫЙ САХАР) С12Н22О11
Молекула сахарозы состоит из остатков α-глюкозы и β-фруктозы, соединенных друг с другом.
Чистая сахароза — бесцветное кристаллическое вещество сладкого вкуса, хорошо растворимое в воде.
В молекуле сахарозы нет открытой (альдегидной) формы. Вследствие этого сахароза не вступает в реакции альдегидной группы – с аммиачным раствором оксида серебра с гидроксидом меди при нагревании.
Подобные дисахариды называют невосстанавливающими, т.е. не способными окисляться.
2. МАЛЬТОЗА.
Это дисахарид, состоящий из двух остатков α-глюкозы, она является промежуточным веществом при гидролизе крахмала.
Мальтоза — является восстанавливающим дисахаридом и вступает в реакции, характерные для альдегидов.
2. Окисление восстанавливающихся дисахаридов
СВОЙСТВА ПОЛИСАХАРИДОВ.
это природные высокомолекулярные углеводы, макромолекулы которых состоят из остатков моносахаридов.
Основные представители — КРАХМАЛ И ЦЕЛЛЮЛОЗА (C6H10O5)n
Крахмал состоит из остатков α-глюкозы, а целлюлоза – из β-глюкозы, которые являются пространственными изомерами и отличаются лишь положением одной гидроксильной группы (выделена цветом):
КРАХМАЛ.
Крахмалом называется смесь двух полисахаридов, построенных из остатков циклической α-глюкозы. Крахмал — белый порошок, нерастворимый в холодной воде.
В горячей воде он набухает и образует клейстер. В отличие от моно- и олигосахаридов полисахариды не обладают сладким вкусом
2. Гидролиз крахмала
(ферментативный или кислотный) – ведет к образованию глюкозы.
3. Крахмал не дает реакции «серебряного зеркала» и не восстанавливает гидроксид меди (II)
4. Качественная реакция на крахмал — окрашивание поверхности в синий цвет при добавлении раствора йода.
ЦЕЛЛЮЛОЗА
наиболее распространенный растительный полисахаридМолекулярная масса целлюлозы — от 400 000 до 2 млн.
Чистая целлюлоза — твердое белое вещество, имеющее волокнистую структуру. Она нерастворима в воде и органических растворителях, но хорошо растворяется в аммиачном растворе гидроксида меди (II). Как известно, сладкого вкуса целлюлоза не имеет.
Цепи целлюлозы построены из остатков β-глюкозы и имеют линейное строение.
ОБРАЗОВАНИЕ СЛОЖНЫХ ЭФИРОВ.
2. Нитрование целлюлозы
Так как в звене целлюлозы содержится 3 гидроксильные группы, то при нитровании избытком азотной кислоты возможно образование тринитрата целлюлозы, взрывчатого вещества пироксилина:
3. Взаимодействие с уксусной кислотой
Образуется ацетат целлюлозы — ацетатное волокно.
4. Гидролиз целлюлозы (ферментативный или кислотный) — образуется глюкоза
БЕЛКИ (ПОЛИПЕПТИДЫ) — биополимеры, построенные из остатков α-аминокислот, соединенных пептидными (амидными) связями.
Формально образование белковой макромолекулы можно представить как реакцию поликонденсации α-аминокислот
Молекулярные массы различных белков (полипептидов) составляют от 10 000 до нескольких миллионов.Макромолекулы белков имеют стереорегулярное строение, исключительно важное для проявления ими определенных биологических свойств.
Несмотря на многочисленность белков, в их состав входят остатки не более 22 α-аминокислот.
По физическим свойствам белки делят на два класса:
1.ГЛОБУЛЯРНЫЕ БЕЛКИ- растворяются в воде или образуют коллоидныеnрастворы
2.ФИБРИЛЛЯРНЫЕ БЕЛКИ в воде нерастворимы
ДЕНАТУРАЦИЯ БЕЛКА
разрушение вторичной и третичной структуры белка с сохранением первичной структуры. Происходит при нагревании, изменении кислотности среды, действии излучения.
Пример денатурации — свертывание яичных белков при варке яиц.
ДЕНАТУРАЦИЯ БЫВАЕТ ОБРАТИМОЙ И НЕОБРАТИМОЙ.
Необратимая денатурация может быть вызвана образованием нерастворимых веществ при действии на белки солей тяжелых металлов — свинца или ртути.
3. КАЧЕСТВЕННЫЕ РЕАКЦИИ НА БЕЛКИ:
1)Биуретовая реакция – фиолетовое окрашивание при действии на белки свежеосажденного гидроксида меди (II).
2) Ксантопротеиновая реакция — желтое окрашивание при действии на белки концентрированной азотной кислоты.
3) Реакция с щелочью в присутствии солей свинца – при нагревании выпадает черный осадок PbS, что свидетельствует о присутствии серосодержащих аминокислот.







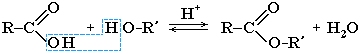
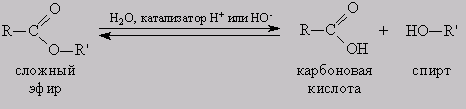
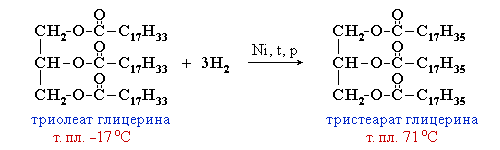
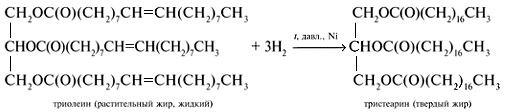



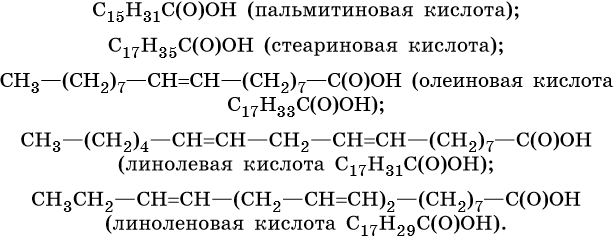
![[[pictureof]]](https://dist-tutor.info/s3/dist-tutor/user/20094/ava/thumbnails/mQ6siSVtAT1Szar.jpg)

































